|
|
МЕНЮ
|
Дипломная работа: Параметры функционирования митоКАТФ у животных с различной устойчивостью к гипоксии, а также у крыс, адаптированных к кислородному голоданию
 
Рисунок 17. А. ДСН-электрофорез фракций 1 – очищенный АТФ-чувствительный К+-транспортирующий белок с м.м. 55 кДа, 2 – молекулярные стандарты массы белков, 3 – суммарный белок МХ. Б. Вестерн-блот анализ: 1 – очищенный АТФ-чувствительный К+-транспортирующий белок с м.м. 55 кДа, 2 – суммарный белок МХ. Показано, что полученные в работе антитела специфически связываются только с белком с м.м. 55 кДа, и не вязываются ни с одним из массы белков, находящихся в МХ (Рис.19). Таким образом, в работе были получены специфические поликлональные антитела на белок с м.м. 55 кДа. Этим же методом было установлено, что поликлональные антитела на исследуемый белок-канал, полученный из МХ печени крысы, не взаимодействует с той же концентрацией аналогичного белка с м.м. 55 кДа, выделенного тем же методом из МХ сердца крысы. Данный факт указывает на то, что исследуемый белок с м.м. 55 кДа тканеспецифичен. 5.4.2 Выделение иммуноглобулинов G (IgG) из антисыворотки и проведение ингибиторного анализаПолученные антитела к АТФ-чувствительному К+-транспортирующему белку с м.м. 55 кДа, выделенному из МХ печени крысы, использовали в качестве ингибитора АТФ-зависимого транспорта ионов калия в МХ печени крысы. Для этого, полученные очищенные и концентрированные антитела (иммуноглобулины G (IgG)) кроликов (см. «Материалы и методы»). Контролем служили очищенные IgG сыворотки крови Интактных (неиммунизированных) кроликов. Кроме того, в качестве контроля использовались антитела к белку с м.м. 55 кДа, подвергнутые кипячению в течение 5 минут. Ранее было показано, что такая процедура ведет к потере белком активности. IgG контрольных животных получали тем же способом, что и IgG рабочей сыворотки. В ходе выделения и очистки IgG титр антител и сродство к белку-каналу с м.м. 55 кДа существенно не изменяется. Степень чистоты выделенных из сыворотки IgG определяли методом ДДС-ПААГ электрофореза [Laemmli, 1979] (см. «Материалы и методы»). Очищенные фракции IgG, выделенные из иммунизированных и интактных животных, использовали для ингибирования АТФ-зависимого выхода ионов К+ из МХ в присутствии ДНФ, отражающего работу митоКАТФ, и энергозависимого входа ионов К+ в МХ. Все эксперименты проводились при термостатировании (26°С) и постоянном перемешивании. После 1.5-2 минут преинкубации антител с митохондриями транспорт ионов К+ индуцировали ДНФ (при исследовании выхода К+ из МХ К+-селективным электродом) или субстратом дыхания (при определении энергозависимого входа К+ в МХ). Для повышения эффективности взаимодействия IgG с внутренней мембраной МХ создавались гипотонические условия. На рисунке 6 представлена концентрационная зависимость степени ингибирования выхода ионов К+ из МХ печени крысы в присутствии разобщителя (ДНФ). Ингибирующий эффект антител наблюдается только в случае добавления в среду инкубации МХ очищенных интактных IgG к АТФ-зависимому К+-транспортирующему белку с м.м. 55 кДа, выделенному из печени крысы. Степень ингибирования зависела от концентрации IgG и времени преинкубации.
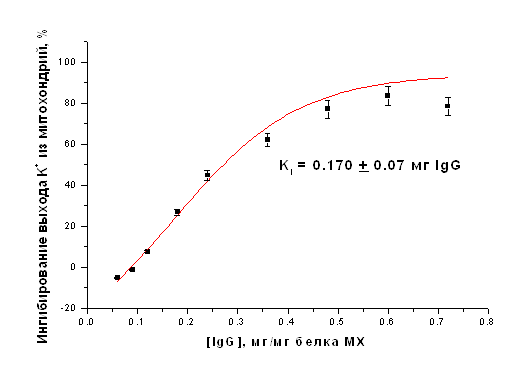
Рисунок 18. Ингибирование АТФ-зависимого ДНФ-индуцированного выхода К+ из МХ печени крысы антителами на АТФ-чувствительный К+ белок-канал с м.м. 55 кДа. Кi = 0.170+0.07 мг IgG/мг белка МХ Максимальное ингибирование, наблюдавшееся в данных экспериментах составляло 83%. Константа полумаксимального ингибирования (Кi) составила 0.170+0.07 мг IgG/мг белка МХ (Рис. 20). Антитела к белку с м.м. 55 кДа, выделенному из МХ печени крысы, ингибируют также энергозависимый вход ионов К+ (Рис. 21).
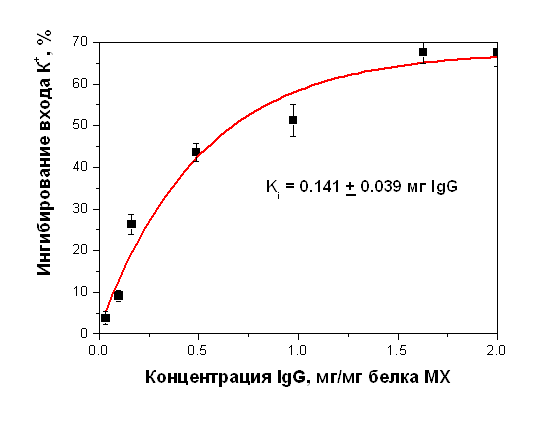
Рисунок 19. Ингибирование энергозависимого входа ионов К+ в МХ печени крысы антителами на белок с м.м. 55 кДа Следует отметить, что IgG контрольной сыворотки и IgG, инактивированные кипячением, не влияли ни на ДНФ-индуцированный выход калия из МХ, ни на энергозависимый вход ионов (Таблица 9). Кроме того, антитела, полученные на АТФ-зависимый К+-транспортирующий белок с м.м. 55 кДа, выделенный из МХ печени крысы, не блокировали АТФ-чувствительный К+ транспорт в МХ сердца крысы, при использовании обоих методов исследования (Таблица 9). Таблица 3. Процент максимального ингибирования АТФ-зависимого К+ транспорта в МХ печени и сердца крыс антителами, полученными на белок с м.м. 55 кДа, выделенный из МХ печени крысы.
В работе также определяли влияние полученных антител на параметры дыхания МХ. Ни контрольные IgG, ни IgG, специфические к белку-каналу с м.м. 55 кДа (Рис. 22), ни инактивированные IgG, не оказывали заметного влияния на дыхание МХ в присутствии субстрата и АДФ. Отсутствие подобного влияния связано, по-видимому, с тем, что в интактных МХ, в которых не индуцировали транспорт К+, роль данного иона в процессе дыхания незначительна. Таким образом, в работе получены специфические поликлональные антитела на выделенный из МХ печени крысы белок с м.м. 55 кДа, формирующий при встраивании в БЛМ АТФ-ингибируемые К+-селективные каналы. Данные антитела блокируют АТФ-зависимый вход К+ в нативные МХ и ДНФ-индуцированный, ингибируемый АТФ, выход этого иона из МХ. Следует отметить, что исследуемые антитела не влияют на другие параметры функционирования МХ, в том числе, на дыхание. Полученные результаты доказывают, что белок с м.м. 55 кДа действительно участвует в формировании АТФ-зависимого калиевого канала внутренней мембраны МХ и, по всей видимости, является его канальной субъединицей. 5.5 Электронная микроскопия МитоКАТФ каналаДля более точного доказательства локализации белка с м.м. 57 кДа во внутренней мембране митохондрий было проведено электронно-микроскопическое исследование срезов тканей печени и сердца с использованием АТ на белок с м.м. 55 кДа. Идентификации эндогенного белка-канала и его связывание с АТ проводились с помощью вторичных антител, меченых коллоидным золотом (диаметр гранул – 10 нм). Как видно из рисунка 21, такого рода гранулы золота локализуются во внутренней мембране митохондрий как печени (Рис.21а), так и сердца (Рис.21б), причем в сердце их больше, что соответствуют данным о большей плотности митоКАТФ каналов в митохондриях сердца. Локализуются эти каналы ближе к месту контакта внутренней и внешней мембраны митохондрий, что особенно проявляется с митохондриях сердца (Рис.21б).
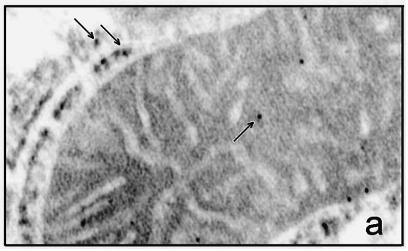
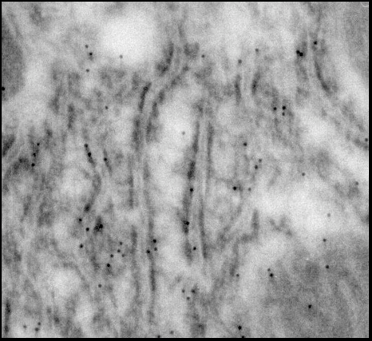
Рис.21а. Электронная микроскопия среза гепатоцита крысы. а - Срезы инкубированы с антителами к митохондриальному К+-транспортирующему белку. Черные гранулы (указаны стрелкой) -сайты локализации К+-транспортирующего белка с м.м. ~ 55 кДа в митохондриях.
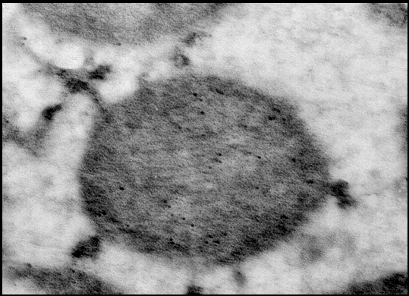
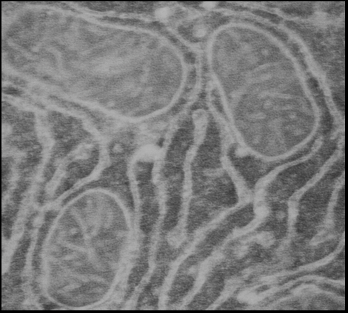
Рис.21 б. Митохондрии и саркоплазматический ретикулум (СР) на срезе кардиомицитов крысы. Срезы инкубированы с антителами к митохондриальному К+-транспортирующему белку. Черные гранулы- сайты локализации К+-транспортирующего белка с м.м. ~ 57 кДа в митохондриях, а также сайты связывания антител с СР. Такие же гранулы (Рис.21А) обнаружены и в ретикулюме, особенно в месте его слияния с мембраной митохондрий, что подтверждает выявленную нами методом MS-MALDI-TOF/TOF – анализа общность в структуре изучаемого белка с микросомах кальретикулином (м.м. 55 кДа).
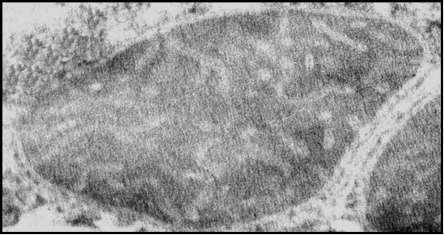
Рис.22. Электронная микроскопия эндоплазматический ретикулум (ЭР) на срезе гепатоцитов крысы. Срезы инкубированы с антителами к митохондриальному К+-транспортирующему белку. В контрольных экспериментах, где были использованы только вторичные АТ, гранулы коллоидного золота не были выявлены. Использование антител к канальной субъединице цитоплазматического КАТФ канала – KIR6.2 не обнаружило наличия этого белка-канала в митохондриях (Рис.23, 24).
Рис.23. Электронная микроскопия среза гепатоцита крысы. Контроль (Первичные антитела заменены буфером).
Рис.24. Митохондрии и
саркоплазматический ретикулум (СР) на срезе кардиомицитов крысы. б - Контроль
(Первичные антитела заменены буфером) Т.о., полученные результаты показали отсутствие общности в структуре KIR6.2 и изучаемого нами митохондриального белка-канала. Приведенные в настоящей работе данные позволяют подтвердить, высказанное нами ранее предположение, что белок с м.м. 55 кДа относится к митохондриальной системе АТФ-зависимого транспорта калия и вместе с известными в литературе глибенкламид-связывающими белками митохондрий входит, вероятно, в состав митохондриального АТФ-зависимого калиевого канала, являясь его канальной субъединицей (митоKIR). ЗАКЛЮЧЕНИЕ Настоящая работа посвящена изучению роли митохондриального АТФ-чувствительного калиевого канала (митоКАТФ) в защите сердца от ишемии, формировании адаптации животных к гипоксии, а также исследованию структурной организации данного канала. В представленной работе также была изучена роль митоКАТФ канала в формировании адаптации животных к кислородному голоданию. Для этого использовали крыс, разделенных на две группы (низкоустойчивые и высокоустойчивые) по способности выдерживать подъем на высоту в 11500 м. Кроме того, в работе низкоустойчивые животные, были адаптированы к недостатку кислорода прерывистой нормобарической гипоксической тренировкой. Показано, что у высокоустойчивых животных митоКАТФ канал работает эффективнее, а показатели сопряжения дыхательной цепи были выше, чем у низкоустойчивых. Адаптация низкоустойчивых животных к гипоксии сопровождается сопряжением дыхательной цепи и активацией митоКАТФ канала. В то же время, поскольку набухания, которое, как предполагается, должно следовать за активацией митоКАТФ, не наблюдается, так как количество калия в митохондриях, по нашим данным, не увеличивается, а даже снижается, вероятнее всего, активируется также и система выхода калия из митохондрий (система К+/Н+-обменника). Задачей настоящей работы было также выяснение структурной гомологии белка с м.м. 55 кДа, формирующего канальную субъединицу митоКАТФ канала [Mironova et al., 2004] аминокислотным последовательностям известных белков. Для этого проводился MS-MALDI-TOF/TOF анализ, с последующей обработкой результатов. Было показано, что белок с м.м. 55 кДа обладает высокой (54%) степенью структурной и функциональной гомологии с типичным представителем семейства кальрегулинов. Полученный результат вызвал необходимость дополнительного исследования принадлежности исследуемого белка-канала к семейству митохондриальных белков. Для этого на 55 кДа белок, выделенный из митохондрий печени крысы и формирующий при встраивании в искусственные мембраны АТФ-чувствительный калиевый канал, были получены специфические поликлональные антитела. Вестерн-блот анализ с полученными антителами позволил выявить тканеспецифичность изучаемого белка-канала. Был также проведен ингибиторный анализ АТФ-зависимого транспорта калия в митохондриях, результаты которого показали, что АТ на белок из митохондрий печени крыс ингибировали этот транспорт в митохондриях печени, но не сердца крыс. При этом они не влияли на показатели сопряженного дыхания митохондрий печени крыс. Следовательно, белок с м.м. 55 кДа действительно относится к системе АТФ-чувствительного входа К+ в митохондрии. Для более точного доказательства локализации белка с м.м. 57 кДа во внутренней мембране митохондрий было проведено электронно-микроскопическое исследование срезов тканей печени и сердца с использованием АТ на белок с м.м. 55 кДа. Которое так же подтверждает высказанное ранее предположение. 1. Формирование устойчивости животных к недостатку кислорода, а также адаптация нормобарической гипоксической тренировкой низкоустойчивых животных сопровождается сопряжением дыхательной цепи, активацией митоКАТФ канала и К+/Н+ - обменника. 2. Показано, что белок с м.м. 55 кДа обладает высокой степенью структурной и функциональной гомологии с типичным представителем семейства кальрегулинов. 3. В работе получены специфические поликлональные антитела на белок с м.м. 55 кДа, формирующий при встраивании в искусственную мембрану АТФ-ингибируемые К+ каналы. Ингибиторный анализ АТФ-чувствительного калиевого транспорта в интактных МХ с использованием полученных антител показал, что белок с м.м. 55 кДа относится к системе АТФ-зависимого входа К+ митохондрий. 4. Электронно-микроскопическое исследование срезов тканей печени и сердца крысы после их инкубации с АТ на белок с м.м. 55 кДа, выделенный из внутренней мембраны митохондрий печени показало его принадлежность к системе митохондриального транспорта калия. ЛИТЕРАТУРА гипоксия белок калий антитело 1. Баграмян К., Трчунян А. Особенности структуры и функционирования формиат-водород-лиазы-фермента смешанного брожения у Escherichia coli. // Биохимия, 2003, т. 68, № 11, с. 1445-1458. 2. Баграмян К.А. Электрохимическое исследование протон-транслоцирующей функции гидрогеназы 3. // Биофизика, 2002, т. 47, № 5. с.847-851. 3. Баранова О.В., Скарга Ю.Ю., Негода А.Е., Миронова Г.Д. Ингибтрование адениновыми нуклеотидами ДНФ-индуцированного транспорта калия в митохондриях. // Биохимия, 2000, т. 65, № 2, с. 262-267. 4. Брустовецкий Н.Н., Данилова Л.С., Маевский Е.И., Колаева С.Г. Изменения реакций окислительного фосфорилирования в митохондриях печени крыс и суслтков при адаптации к холоду и в состоянии зимней спячки. // Эволюционные аспекты гипобиоза и зимней спячки. 1986, с. 69-72 5. Долгов В.В., Райскина М.Е., Антонов В.Ф. Действие адреналина на содержание К+ в митохондриях сердца собаки и зависимость транспорта К+ от дыхания и окислительного фосфорилирования. // Биофизика, 1974, т. 19, № 6, с 1025-1029. 6. Зинченко В.П., Кудзина Л.Ю., Евтодиенко Ю.В., Ким Ю.В. Характеристика К+- транспортирующей системы митохондрий при интенсивной мышечной нагрузке. // Биохимия, 1982, т. 47, № 11, с. 1839-1843. 7. Иванов К.П. Современная теория терморегуляции и зимняя спячка. // Эволюционные аспекты гипобиоза и зимней спячки. 1986, с. 49-54. 8. Киракосян Г., Баграмян К., Трчунян А. Окислительно-восствновительные процессы и образование молекулярного водорода бактериями Escherichia coli в гиперосмотической среде. // Биофизика, 2001, т. 46, № 2, с. 245-250. 9. Кондрашова М.Н., Ахмеров Р.Н., Григоренко Е.В., Федотчева Н.И., Миронова Г.Д. Торможение окисления янтарной кислоты как причина снижения теплопродукции при спячке. // Эволюционные аспекты гипобиоза и зимней спячки. 1986, с. 55-60. 10. Кудзина Л.Ю., Юрков И.С., Полтева Н.А., Евтодиенко Ю.В., Кондрашова М.Н. Влияние редокс-состояния дыхательной цепи на проницаемость мембраны митохондрий для ионов калия. // Биохимия. 1981, т.46, с 1807-1814. 11. Ленский А.С., Введение в бионеорганическую и биофизическую химию. М.: Высш. Шк., 1985, 152 с. 12. Мартиросов С.М., Трчунян А.А. Взаимодействие систем транспорта Н+ и К+ у анаэробно и аэробно выщенных E. сoli. // Биофизика, 1986, т. ХХХI, № 3, с. 464-467. 13. Мартиросов С.М., Трчунян А.А. Поглощение К+ у E. Сoli, выращенных в аэробных условиях. // Биофизика, 1986, т. ХХХI, № 4, с. 626-630. 14. Маршанский В.Н., Новгородов С.А., Ягужинский Л.С. Влияние специфических ингибиторов ферментов дыхательной цепи и АТФ-синтетазы на транспорт ионов в митохондриях, индуцированный неферментативными перекисными реакциями. // Биофизика, 1983, т.28, №5, с. 830-834. 15. Маршанский В.Н., Ягужинский Л.С. Влияние субстратов АТФ-синтетазы на индукцию процесса перекисного окисления липидов в митохондриях. //. Биол. мембраны, 1985, т.2, № 11, с. 1081-1086. 16. Миронова Г.Д., Григорьев С.М. Скарга Ю.Ю., Негода А.Е., Коломыткин О.В. // . АТФ-зависимый калиевый канал митохондрий печени крысы. ІІ. Ингибиторный анализ, кластеризация канала. // Биологические мембраны, 1996 б, т. 13, № 5, с. 537-544. 17. Миронова Г.Д., Маслова Г.М., Федотчева Н.И., Миронов Г.П. Участие митохондриальных систем транспорта в термогенезе теплокровных животных. // В сб. : Эволюционные аспекты гипобиоза и зимней спячки. Л.: Наука, 1986, с.64-68. 18. Миронова Г.Д., Проневич Л.А., Федотчева Н.И.,Сирота Т.В., Трофименко Н.В., Миронов Г.П. Системы транспорта катионов в митохондриях. // Митохондриальные процессы во временной организации жизнедеятельности. Пущино, 1978, с. 451-457. 19. Миронова Г.Д., Скарга Ю.Ю., Григорьев С.М., Яров-Яровой В.М., Александров А.В., Коломыткин О.В. АТФ-зависимый калиевый канал митохондрий печени крысы. І. Выделение, очистка и реконструкция канала в БЛМ. // Биологические мембраны, 1996 а, т. 13, № 4, с. 396-403. 20. Миронова Г.Д., Федотчева Н.И., Макаров П.Р., Проневич Л.А., Миронов Г.П. Белок из митохондрий сердца быка, индуцирующий канальную калиевую проводимость бислойных липидных мембран. // Биофизика, 1981, т. 26, с. 451-457. 21. Миронова Г.Д., Федотчева Н.И., Скарга Ю.Ю., Кондрашова М.Н. Транспорт калия и дыхание митохондрий при выходе суслика из состояния зимней спячки. // Механизмы зимней спячки. Пущино, 1987, с. 39-47. 22. Миронова Г.Д., Федотчева Н.И., Скарга Ю.Ю., Копецки Я., Хоуштек И. Сравнительный анализ термогенных систем митохондрий печени и бурой жировой ткани. // Механизмы природных гипометаболических состояний. Пущино, 1991, с. 34-43. 23. Мнацаканян Н., Захарян Э., Баграмян К., Трчунян А. Дитиол-дисульфидные переходы в мембранных транспортных белках у Escherichia coli. // Биологические мембраны, 2002, т. 19, № 2, с. 183-192. 24. Скарга Ю.Ю., Долгачева Л.П., Федотчева Н.И., Миронова Г.Д. Влияние антител к митохондриальному К+- транспортирующему белку на транспорт К+ в митохондриях печени крысы. // Укр. биохим. Журн., 1987, т. 59, № 6, с. 54-59. 25. Смирнова В.Г., Красных Т.А., Октябрьский О.Н. Роль глутатиона при ответе Escherichia coli на осмотический шок. // Биохимия, 2001, т. 66, № 9, с. 1195-1201. 26. Тер-Никогосян В.А., Трчунян А.А., Мартиросов С.М. Характер поглощения К+ у анаэробно выращенных S. Typhimurium. // Биофизика, 1986, т. ХХХI, № 5, с. 825-828. 27. Трчунян А.А., Дургарьян С.С., Оганджанян Е.С., Тер-Никогосян В.А., Варданян А.Г., Оганесян М.И., Петросян Л.С., Ванян П.А., Карагулян Э.А., Мартиросов С.М. Исследование способности анаэробно выращенных бактерий обменивать 2Н+ клетки на К+ среды и поддерживать высокое распределение К+ между клеткой и средой. // Биологические науки, 1986, №12, с. 82-88. 28. Трчунян А., Оганджанян Е.., Саркисян Э., Гонян С., Оганесян А., Оганесян С. Мембранотропные эффекты электромагнитного излучения крайне высоких частот на Escherichia coli. // Биофизика, 2001, т.46, № 1, с.69-76. 29. Федотчева Н.И. Влияние ГТФ на содержание ионов К+ и окисление субстратов в митохондриях бурого жира. // Механизмы природных гипометаболических состояний. Пущино, 1991, с. 43-49. 30. Федотчева Н.И., Мирзабеков Т.А., Миронов Г.П., Миронова Г.Д. Изменения транспорта К+ в митохондриях печени сусликов при зимней спячке. // Укр. Биохим. Журн. 1984, Т. 54, с. 190-193. 31. Чухлова Э.А., Кудзина Л.Ю., Евтодиенко Ю.В. Влияние голодания на содержание и транспорт ионов калия в митохондриях печени крыс. // Укр. биохим. Журн., 1982, т. 54, № 2, с. 190-193. 32. Шортанова Т.Х., Шугалей В.С., Головина Т.Н. Особенности регуляции метаболизма у зимнеспящих. // Эволюционные аспекты гипобиоза и зимней спячки. 1986, с. 40-43. 33.Altshuld R., Hohl Ch., Ansel A., Brierley G. Compartmentation of K+ in isolated adult rat heart cells. // Arch. Biochem. Biophys., 1981, v. 209, № 1, pp 175-184. 34.Ammala C., Moorhouse A., Gribble F., Ashfield R., Proks P., Smith P.A., Sakura H., Coles B., Ashcroft F.M. Promiscous coupling between the sulfonylurea receptor and inwardly rectifying potassium channels. // Nature, 1996, 379:545-548. 35.Bagramyan K., Mnatsakanyan N., Trchounian A. Formate increases the F0F1-ATPase activity in Escherichia coli growing on glucose under anaerobic conditions at slightly alkaline pH. // Biochem. Biophys. Res. Commun., 2003, Jun 27, v. 306(2), p. 361-5. 36.Bernardi P., Azzone G.F. Electroneutral H+-K+ exchange in liver mitochondria. Regulation by membrane potential. // BBA, 1983, V. 724, pp 212-223. 37.Bogacka K., Nojtczak J. On the mechanism of mercurial-induced permeability of the mitochondrial membrane to K+. //FEBS Lett. 1979, V.100, pp 301-304. 38.Brierley G.P., Jurkowitz M., Jung D.W. Osmotic swelling of heart mitochondria in acetate and chloride salts. Evidence for two pathways for cation uptake. // Arch. Biochem. Biophys. 1978, V. 190, pp 181-192. 39.Brierley G.P. Monovalent cation transport by heart mitochondria. // Patology of cell membranes. 1983, №3, p 23-61. 40.Koster JC, Bentle KA, Nichols CG, Ho K. Assembly of ROMK1 (Kir 1.1a) inward rectifier K+ channel subunits involves multiple interaction sites. // Biophys J., 1998, Apr; 74(4), p 1821-1829. 41.Chavez E., Jung D.W., Brierley G.P. Energy-dependence exchange of K+ in heart mitochondria. K+ efflux. // Arch. Biochem. Biophys. 1977, V. 183, pp 460-470. 42.Clement J.P., Kunjilwar K., Gonzalez G., Schwanstecher M., Panten U., Aguilar-Bryan L., Bryan J. Assotiation and stoichiometry of K+-ATP channel subunita. // Neuron. 1997, v.18, p 827-838. 43.Dascal N, Schreibmayer W, Lim NF, Wang W, Chavkin C, DiMagno L, Labarca C, Kieffer BL, Gaveriaux-Ruff C, Trollinger D, et al. Atrial G protein-activated K+ channel: expression cloning and molecular properties. // Proc Natl Acad Sci USA., 1993, Nov 1; 90(21):10235-9. 44.Diwan J.J., Haley T., Sanadi D.R. Reconstitution of transmembrane K+- transport with a 53 kilodalton mitochondrial protein. // Biochem. Biophys. Res. ComMun., 1988, v. 31, p. 224-230. 45.Divan J. J., Tedeschi H. K+ fluxes mitochondrial membrane potential. // FEBS Lett. 1975, V.60, pp 176-179. 46.Garlid K.D. On the mechanism of regulation of the mitochondrial K+/H+ exchnger. // J. Biol. Chem. 1980, V. 255, pp 11273-11279. 47.Garlid K.D., Paucek P., Korcakova B., Woldegiorgis G. and Mironova G. Differential regulation of K flux through the reconstituted K-ATP channels from cardiac mitochondria and sarcolemma. // ATP-sensitive K+ channels and sulfonylurea receptors. Houston, 1993, p. 81-85. 48.Garlid K.D., Paucek P., Yarov-Yarovoy V., Murrey H.N., Darbenzio R.B., D’Alonzo A.J., Lodge N.J., Smith M.A., Grover G.J. Cardioprotective effect of diazoxide and its interaction with mitochondrial ATP-sensitive K+ channels. Possible mechanism of cardioprotection.// Circ. Res., 1997 V 81, pp. 1072-1082. 49.Gomez-Puyou A., Tuena de Gomez-Puyou M. Monovalent cations in mitochondrial oxidative phosphorilation. // J. Bioenerg. Biomembr., 1977, v.9, № 1, pp 91-102. 50.Grigoriev, S.M., Skarga, Y.Y., Mironova, G.D. and Marinov, B.S. Regulation of mitochondrial KATP channel by redox agents. // Biochim Biophys Acta, 1999, v 1410, p 91-96. 51.Halestrap A.P., Davinson A.M. Inhibition of Ca2+-induced large-amplitude swelling of liver and heart mitochondria by cyclosporin is probably caused by the inhibitor binding to mitochondrial-matrix peptidyl-prolyl cis-trans isomerase and preventing it interacting with the adenine nucleotide translocase. // Biochem. J., 1990, V. 268, pp 153-160. 52.Halestrap A.P. The regulation of oxidation of fatty acids and other substrates in rat heart mitochondria by changes in the matrix volume induced by osmotic strength, valinomycin and Ca2+. // Biochem. J., 1987, V 244, pp159-164. 53.Ho K. The ROMK-cystic fibrosis transmembrane conductance regulator connection: new insights into the relationship between ROMK and cystic fibrosis transmembrane conductance regulator channels. // Curr Opin Nephrol Hypertens., 1998, Jan; v.7(1), p 49-58. 54.Inagaki N., Gonoi T., Clement J.P., Wang C.Z., Aguilar-Bryan L., Bryan J., Seino S. A family of sulfonylurea receptor determines the pharmacological properties of ATP-sensitive K+ channels. // Neuron. 1996, v.16, № 5, p 1011-1017. 55.Inoue I., Nagase H., Kishi K., and Higuti T. ATP-sensitive K+ channel in the mitochondrial inner membrane. // Nature, 1991, v 352, p. 244-247. 56.Yokoshiki H., Sunagava M., Seki T., Sperelakis N. ATP-sensitive K+-channels in pancreatic, cardiac, and vascular smooth muscle cells. //Am. J. Physiol., 1998, v. 274, p. 25-37. 57.Koster JC, Bentle KA, Nichols CG, Ho K. Assembly of ROMK1 (Kir 1.1a) inward rectifier K+ channel subunits involves multiple interaction sites. // Biophys J., 1998, Apr; 74(4), p 1821-1829. 58.Kraegeloh A, Amendt B, Kunte HJ. Potassium transport in a halophilic member of the bacteria domain: identification and characterization of the K+ uptake systems TrkH and TrkI from Halomonas elongata DSM 2581T. // J. Bacteriol. 2005, Feb; v. 187, № 3, p 1036-1043. 59.Kubo Y., Baldwin T.J, Jan YN, Jan L.Y. Primary structure and functional expression of a mouse inward rectifier potassium channel. // Nature, 1993, Mar 11, v. 362(6416):107-8. 60.Kubo Y., Reuveny E., Slesinger P.A., Jan Y.N., Jan L.Y. Primary structure and functional expression of a rat G-protein-coupled muscarinic potassium channel. // Nature, 1993, Aug 26, 364(6440): 758-9. 61.Liu Y., Sato T., O`Rourke B, Marban E. Circulation. Mitochondrial ATP-dependent potassium channels: novel effectors of cardioprotection? // Circulation, 1998, V. 97, pp. 2463-2469. 62.Mitchell P. Coupling of phosphorylation to electron and hydrogen transfer by a chemostatic type of mechanism. // Nature. 1961, V.191, pp 144-148. 63.Mitchell P., Moyle J. Respiration-driven proton translocation in rat liver mitochondria. // Biochem. J., 1971. V. 105, pp 1147-1162. 64.Mitchell P., Moyle J. Translocation of some anions, cations and acids in rat liver mitochondria. // Eur. J. Biochem., 1969, V.9, pp 149-155. 65.Paucek P., Mironova G., Mahdi F., Beavis A.D., Woldegiorgis G., and Garlid K.D. Reconstitution and partial purification of the glibenclamide-sensitive, ATP-dependent K+ channel from rat liver and beef heart mitochondria. // J. Biol. Chem, 1992, v 267, p. 26062-26069. 66.Rhoads D., Epstein W. Cation Transport in Escherichia coli. IX. Regulation of K+ transport. // J. of General Physiology, 1978, v. 72, p. 283-295. 67.Rottenberg H. The mechanism of energy-dependence ion transport in mitochondria. // J. Membr. Biol. 1973, V. 11, pp 117-137. 68.Scarpa A. Transport across mitochondrial membranes. // Membrane transport in biology. 1979, V. 2, pp 263-355. 69.Shears S.B., Brouk S.R. Ion transport difference in liver mitochondria from normal and thyroxine-treated rats. // J. Bioenerg. Biomembr., 1980, v. 12, № 5/6, p 379-393. 70.Shears S.B., Brouk S.R. The influence of thyroxine administered in vivo on the transmembrane protonic electrochemical potential difference in rat liver mitochondria. // Biochem. J., 1979, v. 178, № 3, p. 505-507. 71.Tedeschi H. The transport of cations in minochondria. // BBA. 1981, V.639, p 157-196. 72.Trchounian A, Kobayashi H. Kup is the major K+ uptake system in Escherichia coli upon hyper-osmotic stress at a low pH. // FEBS Lett, 1999, v. 447(23), p. 144-148. 73.Trchounian A, Kobayashi H. K+ uptake by fermenting Escherichia coli cells: pH dependent mode of the TrkA system operating. // Biosci. Rep., 2000, v. 20, № 4, p. 277-288. 74. Trchounian A.A., Ogandjanian E.S. An electrochemical study of energy-dependent potassium accumulation in E. coli. Part XIII. On the interaction of H+-ATPase complex F0F1 with Trk proteins in anaerobically grown cells. // Bioelectr. Bioenerg., 1992, v.27, p. 367-372. |