|
|
МЕНЮ
|
Дипломная работа: Параметры функционирования митоКАТФ у животных с различной устойчивостью к гипоксии, а также у крыс, адаптированных к кислородному голоданию3.4 Исследование ДНФ-индуцированного выхода К+ из митохондрий с помощью К+-селективного электрода Функционирование КАТФ-канала в митохондриях оценивали также по инициированной 2,4-динитрофенолом (ДНФ) скорости АТФ- зависимого выхода калия из митохондрий, т.е. создавали условия для работы канала в обратном направлении (Баранова и др, 2000). В среде без субстрата дыхания и калия регистрировали выход калия из митохондрий после добавления разобщителя окислительного фосфорилирования. Выход К+ из митохондрий индуцировали добавлением 50 мкМ 2,4-динитрофенола. Кинетику выхода калия регистрировали с помощью оригинального электрометрического усилителя, который через контроллер L-153 был соединен с компьютером. Измерения производились при постоянном перемешивании. Концентрация митохондриального белка в ячейке составляла 1-1,5 мг/мл. Среда инкубации митохондрий содержала: 170 мМ сахароза, 80 мМ D-маннит, 5 мМ Na2HPO4, 10 мМ Трис-НCl (рН 7.4). 3.5 Реконструкция белка в БЛМ Для реконструкции белка использовали БЛМ, сформированные из смеси 90 % общих липидов мозга быка и 10 % кардиолипина. Плоские бислои формировали методом Мюллера из липидов, растворенных в н-декане (Mueller et al, 1964). Суммарная концентрация липидов в н-декане равна 20 мг/мл. Трансмембранный ток регистрировали при постоянном напряжении на мембране. Проводимость немодифицированной мембраны составляла 1-3 пСм. Раствор белка вводили в буфер, омывающий одну из сторон мембраны. Буфер содержал: 20 мм Tris, 100 мМ KCl (рН 7,4). Регистрацию тока через ионные каналы в мембране проводили при помощи операционного усилителя с высокоомным сопротивлением в цепи обратной связи. Выход усилителя был подключен к компьютеру. Эксперименты проводились при 20-22ºС. 3.6 Иммунноэлектронная микроскопия Ткань печени и сердца фиксировали в 4%-ном растворе параформальдегид/0.05% глутаровый альдегид в PBS – буфере (16.7 мМ Na2HPO4· 12 H2O, 3.3 мМ KH2PO4, 150 мМ NaCl, рН 7,4) в течение 4 ч при 4°С. Обезвоживание в спиртах и пропитку образца смолой LR-White (Sigma, USA) проводили при 4°С. Полимеризацию смолы осуществляли под ультрафиолетом в течение 48 часов при комнатной температуре. Ультратонкие срезы готовили на ультратоме UC6 (Leica, Германия) и помещали на золотые сеточки, покрытые формваровой пленкой и укрепленные углем (Agar). Неспецифическое окрашивание блокировали обработкой раствором, содержащим 3% БСА и 0.5% желатина в течение 1ч. Все дальнейшие процедуры проводили в PBS содержащем 1% БСА и 0.01% тритон Х-100. После каждой инкубации образцы отмывали PBS- буфером, содержащим 0.1% тритон Х-100 и 0.1% глицин и затем в растворе БСА и желатина в течение 20 мин [18]. В качестве первичных антител были использованы полученные нами антитела к митохондриальному К+-транспортирующему белку (в разведении 1:100), инкубацию с которыми проводили в течение ночи при 4°С. После тщательной отмывки сеточки с образцами помещали на каплю вторичных антител, меченных коллоидным золотом с размером гранул 10 нм (Anti-Rabbit IgG, Sigma, USA) и инкубировали в течение 2 часов при комнатной температуре. После отмывки образцы окрашивали уранилацетатом и цитратом свинца и просматривали под электронным микроскопом Tesla BS-500 (Чехословакия). Специфичность метода проверяли заменой первичных антител на буфер. 3.7 MS-MALDI-TOF/TOF- анализ MS-MALDI-TOF/TOF- анализ был выполнен на базе ГУ НИИ биомедицинской химии РАМН им. В.Н. Ореховича. Очищенный митохондриальный К+-транспортирующий белок подвергали ферментативному гидролизу трипсином в денатурирующих условиях в геле. Пептидную смесь из геля экстрагировали ацетонитрил/гидрокарбонат аммонием и затем проводили масс-спектральный анализ на времяпролетном масс-спектрометре Ultraflex (Bruker, Daltonik) в режиме моноизотопической детекции 300-1800 Да. Масс-спектры анализировались через базу данных MSDC и NCBI программой Mascot (http://www.ncbi.nlm.nih.gov). 3.8 Очистка антител к АТФ-зависимому белку с м.м. 55 кДа Для выделения из антисыворотки, содержащей специфические антитела, фракции иммуноглобулинов, использовали методы дробного высаливания, хроматографии и диализа [Антитела. Методы. Изд-во «Мир», 1991, т.1, с.106-107]. Антисыворотку перед высаливанием разводили в 2 раза раствором 0.9% NaCl (рН 7.5). К полученному объему антисыворотки добавляли половинный объем холодного насыщенного раствора сульфата аммония при перемешивании на ледяной бане. Смесь оставляли на 30 минут и затем центрифугировали 20 минут при 5000 g. Осадок растворяли в 0.9% NaCl (рН 7.5). Эту процедуру повторяли 2 раза. Окончательно осадок растворяли в 0.01 М натрий-фосфатном буфере (рН 7.5), содержащем 0.15 М NaCl и диализовали против этого же буфера в течение 18 часов при 4°С. Нерастворившийся осадок удаляли центрифугированием (20000 g, 10 минут). Надосадочную фракцию наносили на колонку (объем 5 см3, диаметр – 1 см, h = 5 см), заполненную ДЭАЭ-целлюлозой (Sigma) и уравновешенную 0.01 М Na-фосфатным буфером (рН 7.5). Элюирование иммунноглобулинов G (IgG) проводили двойным объемом ступенчатого градиента NaCl: 50, 100, 150, 200 мМ. IgG элюировались 50 мМ NaCl. Фракции, содержащие IgG, объединяли и концентрировали с помощью ПЭГ-20000. Полученную фракцию диализовали против 10 мМ Трис-HCl (рН 7.5) в течение ночи при 4°С. Контроль чистоты фракции IgG осуществляли с помощью SDS-PAAG электрофореза [Laemmli, 1979]. 3.9 Очистка антител к АТФ-зависимому белку с м.м. 55 кДа на колонке с иммобилизованным Белком А Перед очисткой иммуноглобулинов в имеющейся сыворотке измеряли концентрацию белка на спектрофотометре Shimadzu UV-2401 РС (Япония) при длине волны 280 нм. Сыворотку разводили 0.1М Na-фосфатным буфером, pH 7.0 до концентрации белка ~2 мг/мл. Разведенную сыворотку, из расчета 20 мг общего белка, наносили на колонку объемом 1 мл, упакованную конъюгированной с белком A (Amersham, Sigma, USA). После нанесения сыворотки колонку промывали тем же буфером до полного отсутствия белка в элюате. Наличие белка в элюате регистрировали при помощи Uvicord S-II LKB (Швеция). IgG элюировали с колонки 0.1М Na-цитратным буфером, pH 3.0. Элюат немедленно титровали 1М Трис-HCl, pH 9.0 до pH 7.0. Затем колонку отмывали 0.1 М Na-фосфатным буфером до pH 7.0. Концентрацию белка в элюате измеряли на спектрофотометре Shimadzu UV-2401 РС (Япония) при длине волны 280 нм. Чистота IgG проверялась при помощи денатурирующего электрофореза в полиакриламидном геле по методу Лэммли [16]. Очищенные IgG разводили глицерином в соотношении 1:1 и хранили при температуре -20ºС. 3.10 Ингибиторный анализ с использованием антител к белкус м.м. 55 кДаАнализ влияния специфических к белку с м.м. 55 кДа антител на параметры функционирования митоКАТФ канала проводили, во-первых, с использованием К+-селективного электрода, определяя скорость ДНФ-индуцированного выхода К+ из МХ и концентрацию ионов К+ в матриксе МХ (см. п.п. 3.2.). Во-вторых, с помощью определения энергозависимого входа К+ в МХ методом спектрофотометрии (см. п.п. 3.1.). При проведении ингибиторного анализа в качестве контроля использовалась преимунная сыворотка, а также сыворотка, содержащая специфические антитела на белок с м.м. 55 кДа, подвергнутая предварительно 5-тиминутному кипячению. Также определялось влияние антител на процесс дыхания МХ. Глава 4. Выделение комплекса цитоплазматических мембран и микросом печени крыс Для выделения комплекса цитоплазматических мембран и микросом печени использовали самцов крыс альбиносов линии Вистар, массой ~250г. Крыс умерщвляли декапитацией без наркоза. Печень извлекали и помещали в предварительно взвешенную среду выделения (t 0°С). После определения массы и проведения перфузии 0.9% NaCl, печень продавливали через пресс и гомогенизировали в стеклянном гомогенизаторе с тефлоновым пестиком в 8-кратном объеме среды выделения, отнесенном к исходному весу ткани. Сначала осаждали МХ дифференциальным центрифугированием, супернатант центрифугировали на 105000 g 1 час, получившийся осадок наносили на градиент (20, 25, 30, 35% сахароза) крутили 105000g 1 час. Происходило разделение образца на две четкие зоны, 25-30% микросомы, 20% мембраны. 4.1 Метод отбора высоко- и низкоустойчивых животных Схема, по которой животные тестировались на устойчивость к гипоксии, была разработана проф. Лукьяновой [Лукьянова и др., 1999; Лукьянова, Коробков, 1981]. В работе использовались самцы крыс линии Вистар массой 250-300 г., которых помещали в барокамеру. Группа высокоустойчивых (ВУ) – животные, которые выдерживали острую гипобарическую гипоксию, соответствующую подъему на высоту 11500 м, в течение 10-15 мин. Группа низкоустойчивых (НУ) животных выдерживала эту высоту только в течение 1-1.5 мин. Глава 5. Результаты и обсуждения 5.1 Параметры функционирования митоКАТФ канала у крыс с различной резистентностью, а также у животных, адаптированных к гипоксии В этом разделе работы исследовались такие показатели, как дыхание МХ, скорость АТФ-зависимого К+ транспорта, количество К+ в МХ, а также чувствительность этого транспорта к АТФ у крыс с различной резистентностью к гипоксии. 5.1.1 Изучение параметров дыхания и окислительного фосфорилирования в МХ печени и сердца крыс с различной резистентностью к гипоксииНесмотря на то, что участие митоКАТФ в защите миокарда и других тканей от ишемических повреждений не вызывает сомнений, механизм позитивного действия активаторов этого канала остается неясным. Для изучения этого вопроса в работе исследовались параметры дыхания и окислительного фосфорилирования в МХ печени и сердца крыс с различной устойчивостью к недостатку кислорода, а также у животных, адаптированных к гипоксии. Изучение параметров дыхания и окислительного фосфорилирования МХ печени и сердца крыс с различной устойчивостью к гипоксии показало, что скорость дыхания МХ во всех метаболических состояниях у высокоустойчивых животных значительно ниже таковой у низкоустойчивых (Рис.5). Следует отметить, что высокоустойчивые животные – это животные, которые выдерживали острую гипобарическую гипоксию, соответствующую подъему на высоту 11500 м, в течение 10-15 мин. Группа низкоустойчивых (НУ) животных выдерживала эту высоту только в течение 1-1.5 мин.
Рисунок 5. Скорость дыхания МХ высоко- и низкоустойчивых к гипоксии НУ – низкоустойчивые к гипоксии животные, ВУ – крысы, высокоустойчивые к гипоксии. Концентрация белка в кювете – 1-2 мг/мл. Среда инкубации: 5 мМ Tris-HCl, 200 мМ сахарозы, 50 мМ KCl, 5 мМ NaH2PO4, 3 мкМ ротенона, рН 7.2. Эксперименты проводились в закрытой ячейке при постоянном перемешивании и термостатировании при температуре 26°С. При этом измерение дыхательного контроля времени фосфорилирования АДФ показало, что окислительное фосфорилирование, то есть синтез АТФ происходит более эффективно у высокорезистентных крыс (Рис.6).
Рисунок 6. Дыхательный контроль и время фосфорилирования МХ крыс с различной устойчивостью к гипоксии ВУ – высокоустойчивые к гипоксии крысы, НУ – низкоустойчивые к гипоксии животные. Условия как на рис. 7. Это свидетельствует об исходно меньшей экономичности процесса синтеза АТФ у низкоустойчивых животных. Таким образом, гипоксия, т.е. увеличение функциональной нагрузки на дыхательную цепь МХ при подъеме животных на высоту или при подаче воздуха со сниженной концентрацией кислорода, может привести к истощению резервных возможностей дыхательной цепи, что не происходит у высокоустойчивых животных. Адаптация низкоустойчивых крыс интервальной нормобарической гипоксией по методу, предложенному в Hypoxia Medical Academy (США), проявляется у них в сопряжении дыхания, что, в свою очередь, выражается в снижении скорости дыхания, увеличении дыхательного контроля и сокращении времени, необходимого для фосфорилирования АТФ (Рис.9).
Как видно из рис. 7, при адаптации к недостатку кислорода животных низкоустойчивых к гипоксии, скорость дыхания МХ у них уменьшается. Кроме того, у адаптированных крыс сокращается время фосфорилирования и увеличивается значение дыхательного контроля (Рис.9 Б). Эти данные свидетельствуют о возрастании степени сопряженности дыхательной цепи МХ крыс низкоустойчивых к килородному голоданию при гипоксической тренировке. Следовательно, адаптация приводит к переходу крыс из состояния низкой устойчивости в состояние повышеной устойчивости к гипоксии. Согласно данным Лукьяновой [Лукьянова, 2004] при адаптации крыс гипоксической тренировкой время жизни животного при подъеме на высоту, характеризующее общую неспецифическую резистентность крыс, у НУ животных увеличивается уже после первой тренировки на 120-160% (контроль принят за 0). У НУ время жизни в последующие 20 дней превышает исходную резистентность в 2 раза. У ВУ изменения во времени жизни вообще отсутствуют в первые 7 дней, после чего наблюдается небольшое увеличение, максимум до 40%. В работе делается вывод, что при адаптации гипоксической тренировкой наблюдается экономизация энергетических процессов МХ (Рис. 8).
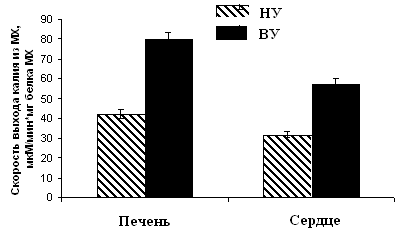
Рисунок 8. Динамика изменения устойчивости к кислородной недостаточности при гипоксической тренировке животных с различной устойчивостью к гипоксии Н/У – низкоустойчивые крысы, В/У – высокоустойчивые, С/У – животные со средней степенью устойчивости (выдерживающие подъем на высоту в 11500 м в течение 7 минут) [Лукьянова, 2004]. В случае, когда такая оптимизация уже существует, как у высокорезистентных животных, тренировки не приводят к увеличению времени жизни крыс в условиях гипоксии [Лукьянова, 2004]. Поэтому эксперименты по адаптации животных мы проводили на низкоустойчивых к гипоксии крысах. В работе были определены параметры АТФ-ингибируемого энергоависимого входа К+ в МХ крыс с различной резистентностью к гипоксии, а также низкоусточивых крыс после их адаптации интервальной нормобарической гипоксической тренировкой. Как следует из рисунка 9А, скорость входа К+ в МХ высокоустойчивых крыс существенно выше, чем в МХ низкоустойчивых животных.
НУ – низкоустойчивые, ВУ – высокоустойчивые животные. Концентрация МХ белка в ячейке 0.1 мг/мл. Среда инкубации: 50 мМ KCl, 5 мМ HEPES, 5 мМ NaH2PO4, 5мМ янтарной кислоты, 0.5 мМ MgCl2, 0.1 мМ ЭГТА, 5 мкМ цитохрома С, 2 мкM ротенона, 1 мкМ циклоспорина А, рН 7.2. Набухание инициировали добавлением МХ.
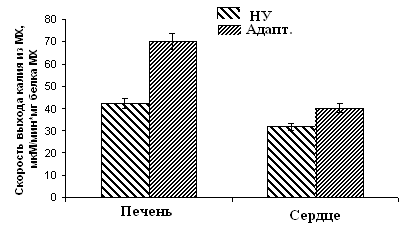
Рисунок 10. Скорость ДНФ-индуцированного выхода ионов К+ из МХ животных высоко-, низкоустойчивых к гипоксии и низкоустойчивых, адаптированных к гипоксии животных ВУ – высокоустойчивые крысы, НУ – низкоустойчивые, Адапт. – низкоустойчивые, адаптированные к гипоксии. Измерения проводились при постоянном перемешивании и термостатировании при 26°С. Концентрация МХ белка в ячейке составляла 1.5-2 мг/мл. Среда инкубации содержала: 0.3 М сахарозы, 3 мМ NaH2PO4, 10 мМ Трис-HCl, pH 7.4. Гипоксическая тренировка приводит к увеличению скорости энергозависимого входа К+ до уровня, сравнимого с аналогичными показателями высокорезистентных крыс (Рис.9Б). Эти данные коррелируют с результатами исследования ДНФ-индуцированного АТФ-зависимого выхода К+ из МХ, измеренного с помощью К+-селективного электрода (Рис. 10). Следует также отметить, что адаптация приводит к изменению параметров ингибирования канала АТФ. Установлено, что Кi для АТФ в митоКАТФ сердца существенно ниже у адаптированных и высокоустойчивых животных, по сравнению с низкоустойчивыми животными (Таблица 1), что является свидетельством более тонкой регуляции К+ транспорта при адаптации крыс к гипоксии. Таблица 1. Константа ингибирования АТФ энергозависимого входа К+ в МХ сердца и печени крыс с различной устойчивостью к гипоксии, а также у адаптированных к гипоксии
* Различия достоверны с p<0.05. При увеличении скорости входа калия в МХ следовало ожидать значительного увеличения количества калия в МХ адаптированных животных, что приводило бы к существенному увеличению объема МХ матрикса. Однако концентрация калия в МХ высокоустойчивых и адаптированных к гипоксии крыс не только существенно не изменилась, но даже уменьшилась (Рис.11А, Б). Это означает, что объем МХ не увеличился, и даже немного сократился. Полученные данные указывают на то, что адаптация, по-видимому, приводит не только к интенсификации энергозависимого входа К+, но и к активации К+/Н+-обменника, который регулирует выход ионов калия из МХ. |
|||||||||||||||
Copyright © 2012 г.
При использовании материалов - ссылка на сайт обязательна.
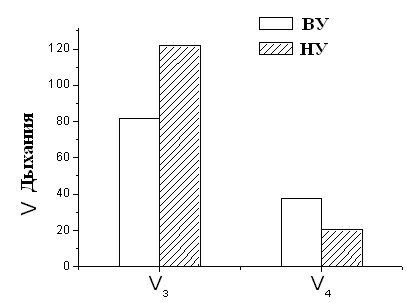
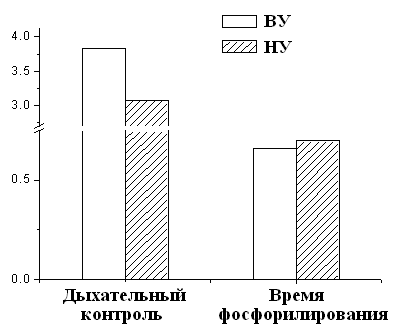
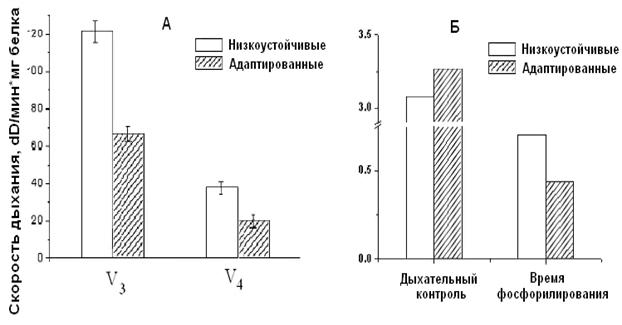 Рисунок 7. Скорость
дыхания (А) и время фосфорилирования (Б) МХ сердца крыс низкоустойчивых и
адаптированных к гипоксии
Рисунок 7. Скорость
дыхания (А) и время фосфорилирования (Б) МХ сердца крыс низкоустойчивых и
адаптированных к гипоксии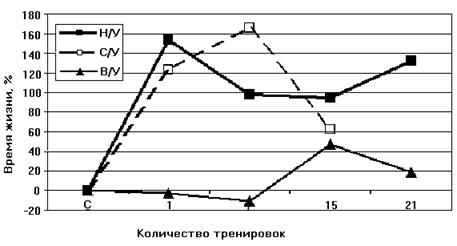
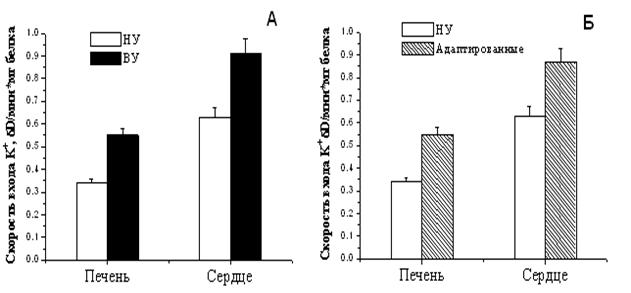 Рисунок 9. Скорость энергозависимого входа
К+ в МХ печени и сердца крыс с различной устойчивостью к гипоксии
(А), а также в МХ животных, адаптированных к гипоксии Б
Рисунок 9. Скорость энергозависимого входа
К+ в МХ печени и сердца крыс с различной устойчивостью к гипоксии
(А), а также в МХ животных, адаптированных к гипоксии Б