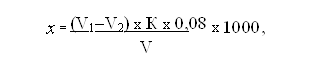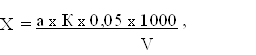|
|
МЕНЮ
|
Дипломная работа: Заболеваемость гипертонической болезнью на территории Шумерлинского района в зависимости от биогеохимических факторовЭкспертами ВОЗ и МОАГ предложена стратификация риска по четырем категориям. Риск в каждой категории рассчитан на основе данных в среднем за 10 лет о вероятности смерти от сердечно-сосудистых заболеваний, а также от инфаркта миокарда и инсульта по результатам Фремингемского исследования. Группа низкого риска (риск 1). Эта группа включает мужчин и женщин в возрасте моложе 55 лет с артериальной гипертензией 1 степени при отсутствии других факторов риска, поражения органов-мишеней и ассоциированных сердечно-сосудистых заболеваний. Риск развития сердечно-сосудистых осложнений в ближайшие 10 лет (инсульта, инфаркта) составляет менее 15%. Группа среднего риска (риск 2). В эту группу входят пациенты с артериальной гипертензией 1 или 2 степени. Основным признаком принадлежности к этой группе является наличие 1-2 других факторов риска при отсутствии поражения органов-мишеней и ассоциированных (сопутствующих) заболеваний. Риск развития сердечно-сосудистых осложнений в ближайшие 10 лет составляет 15-20%. Группа высокого риска (риск 3). К этой группе относятся пациенты с артериальной гипертензией 1 или 2 степени, имеющие 3 и более других факторов риска или поражение органов-мишеней или сахарный диабет. В эту же группу входят больные с артериальной гипертензией 3 степени без других факторов риска, без поражения органов-мишеней, без ассоциированных заболеваний и сахарного диабета. Риск развития сердечно-сосудистых осложнений в ближайшие 10 лет колеблется от 20 до 30%. Группа очень высокого риска (риск 4). К этой группе относятся больные с любой степенью артериальной гипертензии, имеющие ассоциированные заболевания, а также пациенты с артериальной гипертензией 3-й степени с наличием других факторов риска и/или сахарным диабетом даже при отсутствии ассоциированных заболеваний. Риск развития сердечно-сосудистых осложнений в ближайшие 10 лет превышает 30%. Глава 2. Объем и методы исследования В организационно-методическом кабинете Шумерлинской ЦРБ были отобраны статистические талоны по ГБ за три года (2000-2002гг.) (впервые установленные диагнозы) по сельским населенным пунктам. По паспортам участков, журналам диспансерного наблюдения, и картам диспансерного наблюдения (у. ф №30), по амбулаторным картам, на каждый случай заболевания заполнялось карточка с указанием Ф.И.О., года рождения, пола, адреса, места работы, даты взятия на учет, основного диагноза, осложнений, сопутствующих диагнозов. Далее эти данные были занесены в таблицы распределения случаев первичной заболеваемости по населенным пунктам, возрасту, полу (по годам) (таблицы 3.1,3.2,3.3). Используя данные по возрастно-половому составу населения в каждом исследуемом населенном пункте района, были рассчитаны интенсивные показатели заболеваемости по формуле:
Интенсивные показатели первичной заболеваемости рассчитывались по годам и по району в целом. Затем, данные занесли в таблицу первичной заболеваемости по администрациям, полу и годам (таблица 3.4). Далее проведена группировка показателей первичной заболеваемости. Порядок выполненной работы: суммируется годовые показатели по каждой администрации: Мср. = (И.П. 2000 + И.П. 2001 + И.П. 2002)/ 3. За основу группировки берем min и max показатели. Разница между max и min показателями (max – min) является средневзвешенной (С). Max=1,37; min показатель = 0,97. С = 0,40. Определяем границы показателей по пяти группам. III группа – является исходной для расчетов, она среднерайонная с разницей между max и min показателями. III группа – (1,37– 0,97) = 0,40. II группа – выше средней, границы рассчитываем исходя из max показателя с прибавлением 0,01 (max + 0,01). К полученной величине прибавляем средневзвешенную (С). Расчет провели по формуле: Рв/с = (max + 0,01) + С = (1,37 + 0,01) + 0,40 = 1,78 I группа – Рс/в = (Рв/с + 0,01) + С I группа – Рс/в = (1,78 + 0,01) + 0,40 = 2,19 IV группа = ниже средних Рн/с = (min – 0,01) – С IV группа – Рн/с = (0,97 – 0,01) – 0,40 = 0,56 V группа – сверхнизкие Рс/н = (Рн/с – 0,01) – С V группа – Рс/н = (0,56–0,01) – 0,40 = 0,15. Оформляем таблицу равновесных групп по показателям первичной заболеваемости (таблица 3.5). По Шумерлинскому району провели следующую работу: изучили питание семей, уровень субъективной оценки здоровья и выявляли факторы риска развития ГБ опросным методом по анкете "Ваше здоровье, условия и образ жизни", разработанной академиком РЭЛ, профессором, заслуженным деятелем науки Сусликовым В.Л. (приложение 10); изучили условия водоснабжения населения (САН-ПИН 2.14.559-96.). Методика исследования воды. Взятие проб воды для исследования. Воду берут в количестве 2–5л в чистые бутыли, сполоснутые дистиллированной водой и дополнительно той водой, которую берут для анализа. Бутыль с грузом опускают на определенную глубину (на ту, с которой обычно забирают воду), после чего пробку открывают с помощью прикрепленной к ней веревки. Имеются также специальные приборы для забора воды, называющиеся батометрами. Забор воды из колодцев с насосами или водопроводных кранов производят после предварительного откачивания или спуска воды в течение 10–15 минут. После взятия пробы бутыль нумеруют и к ней прилагают сопроводительный бланк с обозначением названия водоисточника, из которого взята проба, места расположения, температуры воды и состояния погоды в момент забора. Определение сухого остатка воды. В кварцевой или фарфоровой чашке, высушенной предварительно до постоянного веса при 110о, выпаривают на водяной бане или электрическом нагревателе 250–500 мл профильтрованной исследуемой воды и чашку с сухим остатком высушивают в сушильном шкафу при 110о до постоянного веса, охлаждая перед каждым взвешиванием в эксикаторе. Разница в весе до и после выпаривания покажет сухой остаток воды. Расчет производят по формуле: Х = (n–n1)х1000/V, где: Х – величина сухого остатка в мг на 1л; n – вес чашки с сухим остатком в граммах; n1 – вес пустой чашки; V – объем воды, взятой для исследования, в мл. С целью получения некоторого представления о содержании в воде органических веществ чашку с сухим остатком прокаливают на пламени горелки до полного сгорания органических веществ, пока осадок не станет белым. После этого прибавляют несколько капель 25% раствора углекислого аммония для превращения разложившихся углекислых солей в углекислые и вновь прокаливают до постоянного веса. Вычитая из веса сухого остатка вес его после прокаливания, получают величину, характеризующую потерю при прокаливании, которая и дает представление о количестве органических веществ. Определение окисляемости воды. В коническую колбу емкостью 250 мл наливают 100 мл испытуемой воды, добавляют 5мл 25% серной кислоты, 10 мл 0,01 н. раствора марганцовокислого калия и, накрыв колбу часовым стеклом, нагревают жидкость до кипения, опустив в колбу несколько стеклянных капилляров. После 10-минутного кипячения вносят в колбу 10 мл 0,01 н. раствор щавелевой кислоты, перемешивают содержимое и обесцвеченный горячий раствор титруют 0,01 н. раствором марганцовокислого калия до появления слабо розового окрашивания. Расчет окисляемости в мг/л кислорода производят по формуле:
где: х – искомая окисляемость воды в мг/л кислорода; V1 – общее количество 0,01 н. раствора марганцовокислого калия, израсходованное при определении окисляемости, в мл; V2 – количество 0,01 н. раствора марганцовокислого калия, израсходованное на окисление 10 мл 0,01 н. раствора щавелевой кислоты, в мл; К – поправочный коэффициент титра раствора КМnО4; 0,08 – количество кислорода, выделяемое 1 мл н. раствора марганцовокислого калия; V – объем воды в мл, взятый для исследования. Определение аммиака (азота аммонийных солей). В цилиндр №1 наливают 100 мл испытуемой воды, а во все остальные цилиндры колориметра – стандартный раствор хлористого аммония, содержащий в 1 мл 0,01 мг N, в цилиндр №2 – 0,5 мл; в цилиндр №3 – 1мл; в цилиндр №4 – 1,5 мл и т.д. Затем цилиндры со стандартным раствором NH4CI доводят до 100 мл дистиллированной водой и, закрыв пробками, перемешивают. После этого во все цилиндры прибавляют по 2 мл реактива Несслера, вторично взбалтывают и через 10 минут, вынув пробки, смотрят сверху вниз и сравнивают окраску испытуемой воды с окраской шаблонных цилиндров с хлористым аммонием и среди них находят подходящую по интенсивности окраску к испытуемой воде. Допустим, что интенсивность окраски испытуемой воды оказалась одинаковой с окраской в цилиндре №4, содержащем 1,5 мл раствора NH4CI. Следовательно, в 100 мл воды содержится 1,5 х 0,01 = 0,015 мг азота аммиака, а в 1 л – 0,15 мг. Определение азотистой кислоты (азота нитритов). Выпаривают на водяной бане в фарфоровой чашке досуха 10 мл испытуемой воды. По охлаждении к выпаренному остатку прибавляют 1 мл сульфофенолового раствора и растирают стеклянной палочкой; через 5 минут смесь разводят дистиллированной водой (10–20 мл), прибавляют 10 мл 10% аммиака и переливают содержимое чашки в колориметрический цилиндр Генера, ополаскивая при этом чашку 2–3 раза дистиллированной водой, которую также сливают в цилиндр. Объем жидкости в цилиндре доводят дистиллированной водой до 100 мл. При наличии нитратов в воде жидкость приобретает желтый цвет. Одновременно аналогичным образом выпаривают и обрабатывают 1–10 мл стандартного раствора азотнокислого калия; необходимое количество его определяется содержанием нитратов в исследуемой воде, что устанавливается на основании качественной реакции. Определение хлоридов. В колбу или стакан объемом 300–500 мл наливают пипеткой 100 мл испытуемой воды, прибавляют 2 капли индикатора хромовокислого калия и титруют раствором азотнокислого серебра до появления неисчезающей очень слабой красноватой окраски. Допустим, что на осаждение хлоридов, растворенных в 100 мл испытуемой воды, пошло 12,1 мл раствора AgNO3. Т.к. каждый мл приготовленного раствора AgNO3 связывает 0,9 мг хлора, то очевидно, что 12,1 мл свяжут 0,9х12,1 = 10,89 мг хлора, которые содержались в 100 мл испытуемой воды. Если в 100 мл воды содержится 10,89 мг хлора, то в 1 л связанного хлора содержится 108,9 мг. Определение сульфатов. В коническую колбу наливают 200 мл исследуемой воды, нагревают до кипения и добавляют 1мл 2,5 н. раствора соляной кислоты и 0,5 г хромовокислого бария, после чего вновь кипятят 3–4 минуты; жидкость принимает при этом желто-красную окраску. Сняв колбу с нагревательного прибора, нейтрализуют содержимое 5% раствором аммиака, прибавляя его по каплям до перехода окраски в желто-зеленый цвет и установления нейтральной или слабощелочной реакции на лакмус. Остудив жидкость до температуры 15о, вновь проверяют реакцию и переливают содержимое вместе с образовавшимся осадком хромовокислого бария в мерную колбу емкостью 250 мл и доводят до метки дистиллированной водой. Затем, взболтав жидкость, фильтруют ее через складчатый фильтр, отбрасывая первые порции (20–30мл). Из остальной части фильтрата отмеривают 100 мл, наливают в склянку с притертой пробкой, прибавляют 1г сухого Йодистого калия (или 10 мл 10% раствора его) и 5 мл 2,5 н. соляной кислоты и ставят склянку в холодную воду (8–10о) на 20 минут. Выделившийся в процессе этого йод титруют 0,01 н. раствором гипосульфита, добавляя в конце титрования 2% раствор крахмала. Содержание сульфат-иона SO4++ вычисляют в мг на 1 л воды по формуле: Х = n х К х 0,32 х 12,5, где: n – число мл 0,01 н. раствора гипосульфита, израсходованных на титрование; К – поправочный коэффициент к титру гипосульфита; 0,32 – количество мг SO4++, эквивалентное 1 мл 0,01 н. раствора гипосульфита; 12,5 – коэффициент пересчета содержания SO4++ в 100 мл фильтрата на 1л исследуемой воды. Определение жесткости воды из двух источников. В колбу вместимостью 150–200 мл наливают 10 мл исследуемой воды, доводят объем до 100 мл дистиллированной воды, добавляют 5 мл буферного раствора, 5–7 кап. индикатора и медленно титруют при интенсивном взбалтывании раствора трилона Б концентрации 0,05 моль/дм3 до изменения окраски. Если на титрование расходуется более 10 мл трилона Б необходимо взять меньший объем исследуемой воды. Для устранения влияния Zn и Cu к пробе добавляют 1–2 мл сульфата Na. Если после добавления к воде буферного раствора и индикатора жидкость постепенно обесцвечивается, то следует повторить определение с добавлением к воде, до внесения реактивов, 5 капель раствора гидроксил амина. Общую жесткость исследуемой воды в мг-экв вычисляют по формуле:
где: Х – искомая жесткость воды в мг-экв/л; V – объем взятой воды в мл; а – число мл раствора трилона Б, пошедшее на титрование; 0,05 – нормальность раствора трилона Б; К – поправочный коэффициент к раствору трилона Б; 1000 – пересчет на 1 л воды. Определение железа. В коническую колбу наливают 100 мл испытуемой воды, прибавляют 2 мл концентрированной соляной кислоты и несколько кристалликов бертолетовой соли и кипятят 20–30 минут. После этого содержимое колбы охлаждают водой из водопроводного крана, переливают в мерную колбу емкостью 100 мл, сливают туда же дистиллированную воду после ополаскивания первой колбы и доводят объем дистиллированной водой до метки; все содержимое перемешивают. Параллельно с этим в другую мерную колбу емкостью 100 мл вносят пипеткой 1–2 мл стандартного раствора железо-аммиачных квасцов, прибавляют 2 мл HCI и доводят объем до метки дистиллированной водой. После этого в обе мерные колбы добавляют пипеткой по 2 мл 50% раствор роданистого аммония, отчего содержимое второй колбы окрашивается в красный цвет. Перемешав еще раз жидкость в каждой колбе, переливают их в два цилиндра Генера емкостью 100 мл и приступают к колориметрированию, которое производят обычно способом, путем уравнения окрасок стандартного раствора и испытуемой воды. Исследование почвы. Взятие проб почвы для исследования. Отбор проб производят в 3–5 точках по диагонали с участка площадью 25 м2 с глубины 0,25. Пробы берут буравом или лопатой, перемешивают и из проб, взятых с каждого горизонта, составляют среднюю пробу весом около 1 кг, которую помещают в банку с пробкой и отсылают в лабораторию. В лаборатории пробы подвергают анализу в свежем виде или доводят почву до воздушно-сухого состояния путем высушивания на воздухе с просеиванием через сито. Определение органического азота. В колбу приливают 25–30 мл фенолсерной кислоты, отстаивают 0,5–1 час. Затем вносят в колбу 1г цинковой пыли и оставляют стоять 1–2 часа для восстановления нитрофенол в амидофенол; для ускорения окислительных процессов прибавляют катализатор – 1 г CuSO4 и 5 г K2SO4. Затем колбу нагревают, доводя жидкость до кипения. По обесцвечивания жидкости кипячения продолжают в течение часа, после чего охлаждают и в случае кристаллизации прибавляют 10 – 15 мл концентрированной серной кислоты. После этого в колбу прибавляют 250 – 350 мл дистиллированной воды, взбалтывают и добавляют в избытке 50% щелочи. Далее соединяют колбу с каплеуловителем, холодильником и приемной колбы емкостью 300 – 400 мл. В приемник наливают 40 – 50 мл 0,1 н. раствора серной кислоты и 3 капли метилоранжа. Содержимое колбы взбалтывают и нагревают до кипения, с чего начинается отгонка аммиака, которая продолжается 1 – 1,5 часа. Окончание отгонки определяют пробой с красной лакмусовой бумажкой: отсутствие посинения позволяет прекратить отгонку. Серную кислоту в приемнике титруют 0,1 н. раствором едкого натра и по разнице в титре находят количество азота. 1 мл 0,1 н. раствора серной кислоты соответствует 1,4 мг азота. Результат исследования вычисляют по формуле:
где: Х – искомое количество общего азота в мг в 100 г абсолютно сухой почвы; а – разница в титре H2SO4 до и после титрования в мл; 1,4 – количество мг азота, соответствующее 1 мл 0,1 н. раствора H2SO4; б – навеска воздушно-сухой почвы в гр; в – процент гигроскопической воды; 100 – пересчет на 100 г почвы; Определение " почвенного белкового" азота. Берут навеску воздушно-сухой почвы в 3 – 5г, просеянной через сито, насыпают ее в пробирку, взвешивают и пересыпают в химический стакан емкостью 150 – 200 мл. Пробирку вновь взвешивают и по разности между первым и вторым взвешиванием определяют точный вес навески почвы. В стакан с навеской приливают 50 мл дистиллированной воды, взбалтываю, кипятят в течение 5 минут, прибавляют 25 мл 6% раствора медного купороса, перемешивают и приливают 25 мл 1,25% раствора едкого натра. Отстоявшийся осадок промывают 5 – 7 раз горячей водой декантацией, переносят на фильтр и промывают теплой водой. Промытый осадок просушивают вместе с фильтром на воронке в сушильном шкафу, после чего фильтр с осадком переносят в колбу, прибавляют 0,3 г сернокислой меди, 5 – 6 г сернокислого калия, 35 мл чистой концентрированной кислоты и, поступая в дальнейшем также как, при определении общего азота, находят искомое количество "почвенного белкового" азота. Анализ водной вытяжки из почвы. Соли аммиака, азотистой и азотной кислоты, хлориды, сероводород и окисляемость определяют в водной вытяжке теми же способами, что и при анализе воды. Содержание минеральных солей выражается в мг на 1 кг почвы; окисляемость – количество мг кислорода, израсходованного на окисление органических веществ водной вытяжки на 100 г почвы. Глава 3. Собственные исследования. Изучение распространения заболеваемости ГБ на исследуемой территории за 3 года (2000–2002гг.) Первичный собранный материал был разбит по населенным пунктам (деревни и села, объединенные в администрации), по возрастным интервалам и по полу, то есть был объединен в таблицу (см. таблицы 3.1,3.2,3.3,3.4). Таблица 3.1 Первичная заболеваемость ГБ населения Шумерлинского района за 2000 г.
Примечание: Страницы: 1, 2, 3, 4, 5, 6, 7, 8 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Copyright © 2012 г.
При использовании материалов - ссылка на сайт обязательна.