|
|
МЕНЮ
|
Дипломная работа: Методы диагностики и профилактики микробной контаминации при трансплантации эмбрионовВ последние годы в ветеринарной практике широко используется антибиотик гентамицин, который обладает широким антимикробным спектром. Он действует бактерицидно, подавляя синтез белка, ингибируя процессы трансляции и активен по отношению к стафилококкам, эшерихиям и псевдомонадам (А.С. Новохатский и соавт., 1975; Д.Ф. Осидзе, 1981; С.М. Кузнецова, 1983; В.Ф. Ковалев и соавт., 1988). Несмотря на неодобрение многих авторитетов, применение комплекса антибиотиков стало обычным делом в клинической практике. Наиболее хорошо известным примером синергизма между антибиотиками является взаимодействие пенициллинов саминогликозидами. Этот комплекс проявляет синергизм в отношении зеленящих стрептококков, энтерококков, золотистых стафилококков, листерий и грамотрицательных палочек (С.М. Кузнецова, 1983). Механизм синергизма между пенициллинами и аминогликозидами не известен. Он может состоять в увеличении проникновения аминогликозидов в бактериальную клетку в присутствии пенициллина, который ингибирует синтез клеточной стенки, как это было предложено при объяснении действия комбинации пенициллин + аминогликозиды на энтерококки. Однако, независимо от возможного механизма имеющиеся данные показывают, что комбинированное лечение может значительно повысить эффективность антибиотикотерапии инфекций, вызванных Ps. aeruginosa (И.С. Чекман и соавт., 1986; В.Ф. Ковалев и соавт., 1988). Санирующий эффект препарата зависит от дозы: чем больше доза препарата, тем отчетливее выявляется санирующий эффект. Однако увеличение дозы приводит не только к усилению действия препарата, но и к повышению его токсичности (Н.Г. Балашов, 1980). А.С. Новохатский, С.С. Герасимова (1975) изучали цитотоксические свойства гентамицина. Они установили, что гентамицин в концентрации 10, 20 и даже 30 мкг/мл не вызывал нарушений целостности клеточного пласта после 24 часовой инкубации при температуре 37°С. Концентрация 50 мкг/мл и больше приводила к цитотоксическому изменению клеток. А.П. Простяков и С.П. Сергеева (1980) отметили высокую стабильность гентамицина в культуральной среде (6 дней период полураспада), а также цитотоксическую (3000 мкг/мл) и рекомендуемую концентрацию (200 мкг/мл). В опытах Х.Г. Михаеляна (1988) в культуральной среде с концентрацией гентамицина 50 мкг/мл созревание ооцитов достигло 100%, из них 84% клеток созрело до стадии метофазы II, в контроле (без антибиотиков) до этой же стадии созревало только 70%. Для подавления же большинства микроорганизмов достаточна концентрация гентамицина 4 мкг/мл (Д.Ф. Осидзе, В.Ф. Ковалев, К.С. Масловский, 1981). В 1986 г. для санации вымывных буферных сред в лаборатории трансплантации А.Д. Бугровым, И.М. Величко и соавт. предложен и испытан комплекс антибиотиков гентамицин + пенициллин (ампициллин) в концентрациях 12 мкг/мл и 100 Ед/мл, соответственно. Эта комбинация дала хороший антимикробный эффект по отношению к микроорганизмам, встречающимся в половых путях доноров (E.coli, Staph. aureus, Bac.subtilis, Pseudomonas aeruginosa). По данным И.С. Чекмана (1986) гентамицин не совместим с антибиотиками из группы бензилпенициллин, совместим с изотоническим раствором хлористого натрия. При совместном применении гентамицина с ампициллинонатриевой солью, карбенициллином или линкомицином усиливается их антибактериальный эффект. Т.А. Зацепилова и А.Н. Кудрин (1983) установили, что переход лекарственных веществ из жидкости матки через оболочку морулы и бластоцисты зависит от его молекулярной массы. Многие авторы независимо друг от друга определяли влияние антибиотиков на яйцеклетку. Так, М.Ф. Карашаев (1987) установил отрицательное влияние комплекса антибиотиков пенициллин + стрептомицин (100 Ед/мл и 50 мкг/мл) на созревание ооцитов. Таким образом, можно сделать вывод, что применением антибиотиков, как компонентов сред, можно контролировать развитие микрофлоры. Однако не все антибиотики, которые обладают широким спектром антимикробного действия, можно использовать для санации спермы, промывных буферных сред, эмбрионов. Лучшими комплексами антибиотиков для них являются аминогликозиды в сочетании с пенициллинами, примером которых, является гентамицин. Из пенициллинов в комбинации с гентамицином лучше всего сочетается ампициллин. Анализ литературных данных показал, что несмотря на достигнутые успехи в эмбриотрансплантации, проблемными остаются вопросы по приживляемости эмбрионов. Известно много причин, влияющих на приживляемость эмбрионов, одной из которых является микробный фактор. Хотя многие известные ученые не учитывают влияние микрофлоры на жизнеспособность и приживляемость эмбрионов считая, что эмбрионы с интактной зоной пеллюцида надежно защищены от микробов и вирусов. Однако в литературе есть данные о том, что некоторые вирусы и прилипают к прозрачной оболочке и заносятся вместе с эмбрионом в матку реципиента, оказывая негативное влияние на него. Недостаточное количество противоречивых данных о влиянии микроорганизмов на приживляемость эмбрионов стало основанием для проведения исследований по данной проблеме. С целью предупреждения заноса инфекции при трансплантации отечественными и зарубежными учеными разработаны различные технологии, приемлемые в хорошо оборудованных центрах трансплантации эмбрионов. В производственных условиях необходимы дополнительные меры профилактики микробной загрязненности. Известно, что лучшими антимикробными средствами являются антибиотики. Тем не менее, в доступной для нас литературе мало данных о влиянии антибиотиков на эмбрионы. Поэтому перед нами встала задача изучить влияние различных антибиотиков и их доз для профилактики микробной контаминации на всех этапах эмбриотрансплантации. 2. Собственные исследования 2.1 Цель и задачиЦелью нашей работы была разработка методов профилактики и санитарного контроля технологических процессов при трансплантации эмбрионов у крупного рогатого скота. Для достижения этой цели нами поставлены на разрешение следующие задачи: 1. Изучить бактериальную контаминацию половых путей телок-реципиентов в фолликулярную и лютеальную фазы полового цикла. 2. Изучить влияние антибактериальных препаратов на микрофлору половых путей после их санации непосредственно перед извлечением и пересадкой эмбрионов. 3. Провести сравнительную оценку антибактериальных препаратов для санации половых путей. 4. Испытать антибиотики для санации промывных буферных сред и отмывки эмбрионов. 5. Изучить влияние испытанных нами антибактериальных препаратов на жизнеспособность и приживляемость эмбрионов. 2.2 Материалы и методика исследованийВсе исследования по данной работе проводились в лаборатории трансплантации эмбрионов сельскохозяйственных животных Харьковского биотехнологического центра Украинской академии аграрных наук и на пункте трансплантации эмбрионов опытного хозяйства «Кутузовка». Работа выполнялась в период с июля 2000 года по август 2001 года. Пункт трансплантации эмбрионов крупного рогатого скота, построенный по типовому проекту, имеет манеж для санитарной обработки животных перед операцией, операционную, поисковую и стерильный бокс для первичной обработки эмбрионов, помещение для замораживания и хранения эмбрионов, моечную и др. В манеже и операционной расположены специальные фиксационные станки. Операционная, поисковая и стерильный бокс оборудованы бактерицидными лампами. Пункт оснащен необходимым лабораторным, технологическим оборудованием и лабораторной посудой. Предметом исследования были коровы и телки черно-пестрой породы и полученные от них эмбрионы. В опытном хозяйстве «Кутузовка» беспривязная система содержания на глубокой несменяемой подстилке. Кормление животных проводили по общепринятым нормам. Рационы были сбалансированы по общей питательности, белку, фосфору, кальцию и витаминным добавкам. Животные регулярно подвергались ветеринарно-профилактическим и санитарным обработкам, клинико-гинекологическим обследованиям, постоянно находились под ветеринарно-зоотехническим наблюдением. Исследования проводили на коровах-донорах и телках-реципиентах с нормальным состоянием половых органов и цикличностью воспроизводительной функции. Опытная группа состояла из коров в возрасте 3–8 лет, с живой массой 500–600 кг и телок в возрасте 16–18 месяца, с живой массой 350–380 кг. В контрольную группу отбирали коров и телок методом пар-аналогов. В экспериментах использовано 25 коров-доноров и 60 телок – реципиентов. Для вызывания суперовуляции применяли препараты ФСГ. Животные обрабатывались по 4-х дневной схеме ФСГ‑п производства фирм «Schering Corp» или» Burns Biotec» США и ФСГ-супер (Россия) в общей дозе 50 мг (Табл. 1). Таблица 1. Схема гормональной обработки коров-доноров препаратом ФСГ‑п (50 мг) производства США
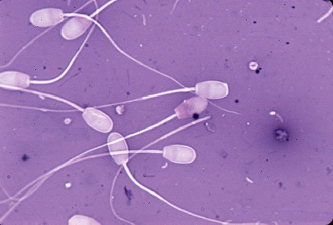
Синхронизация полового цикла доноров и реципиентов осуществлялась инъекцией экстрофана. Осеменение коров-доноров проводилось двукратно двойной дозой замороженно-оттаянной спермы с содержанием не менее 25 млн. активных спермиев (рис. 1). Из спермодозы готовили мазки для определения патологических форм спермиев. Мазки высушивали, фиксировали и окрашивали гематоксилином Караччи. Сперму, содержащую 18% и более патологических спермиев, выбраковывали, так как высокий процент патологических спермиев снижает оплодотворяющую способность спермы.
Рис. 1. Нормальные спермии быка
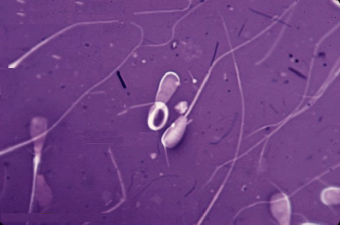
Рис. 2. Патологические формы спермиев
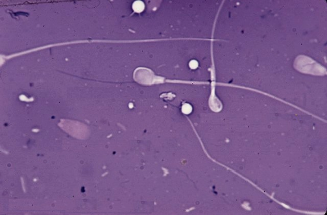
Рис. 3. Патологические формы спермиев
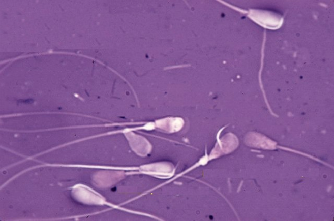
Рис. 4. Патологические формы спермиев Для бактериологических исследований использовали мясо-пептонный агар (МПА) и мясо-пептонный бульон (МПБ), среду Китт-Тароцци, Сабуро и Булира, агар Эндо. МПА и МПБ использовали для культивирования различных микроорганизмов неопределенного состава. Для культивирования анаэробных микроорганизмов использовали среду Китт-Тароцци (МППБ). Среду Булира и агар Эндо применяли для культивирования кишечной палочки. Для выращивания грибов использовали среду Сабуро. Все среды перед бактериологическим исследованием разливали в пробирки по 5 мл. Пробирки закрывали ватно-марлевыми пробками и стерилизовали автоклавированием при температуре 120°С в течение 15–30 минут. МПА после стерилизации скашивали, установив пробирки в наклонном положении до застывания среды. Среду, предназначенную для культивирования бактерий на чашках разливали по 20–25 мл и оставляли на несколько минут до застывания агара. Когда требовалось вырастить микроорганизмы на агарезированной среде в виде изолированных колоний, чашки после засева помещали в термостат дном вверх. Отбор проб для бактериологических исследований проводили на всех этапах подготовки эмбрионов к трансплантации. 2.2.1 Подготовка лаборатории, посуды и инструментов для манипулирования с эмбрионамиВ помещениях лаборатории, где подготавливали инструменты, оборудование, посуду, среды для получения, пересадки и криоконсервации эмбрионов, ежедневно проводили влажную уборку. Все оборудование бокса, его стены, пол не реже одного раза в неделю мыли моющими средствами и протирали дезинфицирующими растворами. Для дезинфекции использовали 2%-й раствор хлорамина «Б». Перед работой бокс и другие помещения лаборатории облучали в течение 40–60 минут ультрафиолетовыми лучами из расчета 2–3 вт/м. В боксе в день работы с эмбрионами проводили дополнительную обработку столов и оборудования 96° этанолом. Все сотрудники лаборатории работали в стерильных халатах и сменной обуви. Спецодежду (халаты, косынки, шапочки, марлевые повязки) стирали не реже одного раза в неделю с обязательным кипячением и проглаживанием утюгом. Обувь регулярно по окончании работы мыли и обеззараживали 2%-м раствором хлорамина. Употребляемые для работы с эмбрионами инструменты, посуду стерилизовали различными способами в зависимости от материала, из которого они изготовлены. Стеклянную посуду (флаконы, колбы, пипетки, цилиндры и пр.), а также инструменты для пересадки эмбрионов закрывали пергаментной бумагой и стерилизовали автоклавированием при 1,5 атм. в течение 30 мин. Затем сушили при температуре 80°С в течение 60 минут. Шприцы, иглы, пинцеты, ножницы, влагалищные зеркала и системы для вымывания эмбрионов стерилизовали кипячением в течение 30 минут. Перед стерилизацией новую стеклянную посуду мыли водопроводной водой с мылом или порошком, с помощью щеток и ершей, ополаскивали и погружали в раствор соляной кислоты (1 ст. ложка соляной кислоты на 3 литра дистиллированной воды) и выдерживали в нем 24 часа. После чего посуду отмывали в проточной воде, а затем многократно в би- и тридистиллированной воде и высушивали. Бывшую в употреблении стеклянную посуду мыли в горячем 2–3% растворе двууглекислой соды, затем тщательноополаскивали водопроводной водой, после чего би- и тридистиллированной водой и высушивали. Бывшие в употреблении металлические предметы также мыли в вышеуказанном растворе соды, ополаскивали водопроводной, би- и тридистиллированной водой и высушивали. Одноразовые полимерные инструменты (ампулы, чехлы, пипетки и др.) стерилизовали в боксе путем их облучения бактерицидными лампами БУФ‑30 или ПРК‑2 в течение 20 мин. с обеих сторон на расстоянии 20 см от источника облучения. Резиновые инструменты (катетер для вымывания) обрабатывали 70°С спиртом-ректификатом. Наружную поверхность стерилизовали, облучая лампами БУФ‑30 в течение 20 мин. на расстоянии 20 см от источника ультрафиолетовых лучей, перед работой ополаскивали 2–3 раза средой Дюльбекко. 4.2.2 Подготовка доноров и реципиентовПодготовку донора начинали в манеже с чистки и мытья кожного покрова и конечностей. Затем животное переводили в операционную, фиксировали в станке, прямую кишку освобождали от содержимого. Для снятия напряжения прямой кишки проводили эпидуральную анестезию 2%-ым раствором новокаина в дозе 5 мл. По инструкции наружные половые органы и перенеальную область тщательно мыли водой с мылом, осушали салфеткой, дезинфицировали аэрозолем «Септонекс» или 70°-м этанолом. В опытах, корень хвоста, область промежности и наружные половые органы тщательно мыли теплой водой с мылом, осушали ватным тампоном. Кожу наружных половых органов и половые пути (преддверие влагалища, влагалище и влагалищную часть шейки матки) орошали раствором Люголя. Для этой цели хвост отводили в сторону вперед, фиксировали его при помощи веревки за переднюю перегородку станка. Во влагалище вводили подготовленное влагалищное зеркало. Через открытое зеркало орошали слизистые оболочки половых путей раствором Люголя. Через 15 минут после санации половых путей проводили извлечение эмбрионов. Подготовку реципиентов к пересадке эмбрионов осуществляли также, как и подготовку доноров для нехирургического извлечения зародышей. Для предотвращения заноса микрофлоры в матку реципиента проводили санацию половых путей раствором Люголя за 15 мин. до пересадки эмбрионов. Приготовление раствора Люголя. Раствор Люголя готовили по следующей прописи: кристаллический йод – 1,0 г йодистый калий – 2,0 г дистиллированная вода – 300,0 мл. 2,0 г йодистого калия растворяли в 100 мл воды, добавляли 1,0 г кристаллического йода и ставили на 10–12 часов в термостат до полного растворения йода. При этом йод растворяется в йодистом калии. Раствор переливали в большую мерную склянку и доводили общий объем до 300,0 мл. Затем его фильтровали и хранили во флаконах из темного стекла. Раствор использовали не более 30 дней. 4.2.3 Извлечение и подготовка эмбрионов к пересадкеИзвлечение эмбрионов проводили на 7-8 день полового цикла нехирургическим методом. Перед операцией донора готовили по методике, описанной в разделе 1.2, затем эпидурально вводили 5–7 мл 2%-го новокаина в зависимости от веса животного. Беспокойным добавочно вводили 0,3–0,5 мл ромпуна. Ректально методом пальпации оценивали состояние полового аппарата, проводили подсчеты желтых тел и фолликулов. Для вымывания эмбрионов использовали катетеры различных конструкций. Промывная жидкость подавалась через закрытую систему самотеком из емкости, расположенной в верхнем гнезде штатива над донором. Промывание маточного рога проводили 8–10 раз, вводя по 60–50 мл промывной среды. На вымывание одного рога расходовали 450–500 мл модифицированной среды Дюльбекко с добавлением 1% инактивированной сыворотки крови крупного рогатого скота. В научно-производственных опытах по санации промывных буферных сред добавляли комплекс антибиотиков гентамицин-ампициллин в концентрациях 12 мкг/мл и 100 Ед/мл, соответственно. Бактерицидную дозу санирующих препаратов испытывали на штаммах микроорганизмов, как монокультуре, так и в ассоциации, методом серийных разведении. Безвредность санирующих препаратов для эмбрионов определяли методом культивирования эмбрионов крупного рогатого скота в средах содержащих различные дозы испытуемых препаратов. |
|||||||||||||||||||||||||||||||||||||||||||
Copyright © 2012 г.
При использовании материалов - ссылка на сайт обязательна.