 |
|
МЕНЮ
|
Реферат: Технічна термодинаміка та теплові процеси технології будівельних матеріалівРеферат: Технічна термодинаміка та теплові процеси технології будівельних матеріалівМіністерство освіти і науки України Національний університет водного господарства і природокористування В.Л. Шестаков Задачі та вправи з технічної термодинаміки та теплових процесів технології будівельних матеріалів Навчальний посібник Рекомендовано Рівне - 2006 УДК 536.7: 621.036; 666.9.013 ББК 38.626.2 - 5873 Ш 52 Рекомендовано Відповідальний редактор: Рецензенти: В.Л. Шестаков Задачі та вправи з технічної термодинаміки та теплових процесів технології будівельних матеріалів. Навчальний посібник. - Рівне: НУВГП, 2006 ISBN 966-7447-99-5 Даний посібник призначений для студентів, які вивчають "Термодинаміка" та "Технологічне обладнання підприємств з виробництва будівельних матеріалів і виробів" за спеціальністю "" Технологія будівельних конструкцій, виробів і матеріалів. Посібник може бути використаний для теплотехнічних розрахунків в курсовому та дипломному проектуванні теплових агрегатів і технологічних ліній з виготовлення будівельних матеріалів, виробів і конструкцій. Для студентів спеціальностей будівельного профілю, також хіміко-технологічних спеціальностей виробництва силікатних будівельних матеріалів. ISBN 966-7447-99-5 УДК 536.7: 621.036; 666.9.013 ББК 38.626.2 - 5873 В.Л. Шестаков, 2006 НУВГП, 2006 ЗмістЗміст Передмова І. Термодинаміка 1.1 Параметри стану робочих тіл (газ, пара) визначаються температурою t, тиском Р, об’ємом V і питомим об’ємом W 1.2 Рівняння стану 1.3 Теплоємність газів. Змішування. 1.4 Аналітичний вираз І законуну термодинаміки має вигляд: 1.5 Процес підведення або відбирання теплоти 1.6 Ентропія згідно із ІІ законом термодинаміки для обернених процесів складає 1.7 Круговий процес або цикл 2. Теплопередача 2.1 Теплопровідність у стаціонарному режимі при сталій температурі 2.2 Нестаціонарномий режим 2.3 Конвективний теплообмін 2.4 Випромінювання газової фази 2.5 Фізичні властивості водяної пари ІІ. Завдання до самостійної роботи Задачі Додатки - таблиці ПередмоваПосібник містить в кожному розділі теоретичні посилання, приклади розв’язання задач і вправ, також перелік задач, вправ і тестів для самостійної роботи студентів і самоконтролю знань з технічної термодинаміки і теплотехніки. В розділі 1 розглядаються теоретичні і практичні питання з технічної термодинаміки, в розділі 2-3 теплопередачі; розділ 3 присвячений розрахункам горіння палива, розділ 4 - розрахункам газодинамічного тракту руху гріючих газів, розділ 5 - теплообміну в теплових апаратах (печі, сушили, установки тепловологісної обробки) виробництва будівельних матеріалів і виробів. Посібник включає необхідні графічні матеріали, таблиці за текстом та значний табличний матеріал в додатках про необхідні теплофізичні характеристики основних газів, повітря, водяної пари, основних видів палива родовищ України, характеристики місцевих опорів руху повітря тощо. Приклади розрахунків в значній мірі адаптовані до теплотехнічних апаратів промисловості будівельних матеріалів та теплових ситуацій, що в них виникають. Задачі і вправи базуються на сучасних технологіях теплової обробки матеріалів з використанням галузевого досвіду з виготовлення цементу, будівельної кераміки, залізобетону та ін. Посібник може бути використаним для проведення теплотехнічних розрахунків в курсовому і дипломному проектуванні теплових агрегатів, комплектуючих технологічні лінії з виготовлення будівельних матеріалів, виробів і конструкцій. І. ТермодинамікаОсновні теоретичні положення. Приклади розв'язання задач з термодинаміки. 1.1 Параметри стану робочих тіл (газ, пара) визначаються температурою t, тиском Р, об’ємом V і питомим об’ємом WАбсолютний тиск в котлах складає: Рабс = Рман+В, у вакуумних установках - Рабс = В - Рман, де Рабс, Рман - показники тиску за показанням манометра або вакуумметра, В - атмосферний (барометричний) тиск. Приведений показник ртутного барометра (до 00С) складає: В0=В (1-0,000172t), (1.1) В - дійсне показання барометра при температурі t0С, 0,000172 - коефіцієнт об'ємного розширення ртуті. Приклад 1-1. Визначити абсолютний тиск пари в котлі, якщо манометр показує Р=0,13 МПа, а атмосферний тиск по ртутному барометру складає В=680мм рт. ст. (90660Па) при t=250С. Рабс = РМАН+В. Показання барометра, приведене до 00С, складає В0 = В (1-0,000172t) = 99660 (1-0,000172∙25) = 90270 Па. Тоді абсолютний тиск пари в котлі Рабс = 0,13 + 0,09 = 0,22 МПа. Приклад 1-2. Тиск у паровому котлі Р = 0,04 МПа при барометричному тиску Во1 = 96660 Па (725 мм рт. ст). Чому дорівнює надлишковий тиск в котлі, якщо показання барометра підвищаться до В02 = 104660 Па (785 мм рт. ст), а стан пари залишиться таким, як був. Барометричний тиск приведений до 00С. Абсолютний тиск в котлі Рабс = 40000 + 96660 = 136660 Па. Надлишковий тиск Рнад = 136660 - 104660 = 0,032 МПа. 1.2 Рівняння стануЯкщо температура газу є сталою (T-const), то згідно закону Бойля-Маріотта РV = const. Якщо тиск газу є сталим (Р = const), згідно закону Гей-Люссана Для газів, які мають однакову температуру і
тиск, на основі закону Авогардо Нормальні умови відповідають тиску Р = 101325
Па, Т = 273,15 К (760 мм рт. ст., 00С). Об’єм 1 кмоля ідеальних
газів = 22,4136 Характеристичне рівняння ідеального газу:
Де R - газова стала, V - об’єм, M - маса газу. Газова стала відносно 1 кг газу складає: Виходячи із характеристичного рівняння дійсним є
Приклад 1-3. Тиск газу за показанням манометра складає 0,3 МПа при температурі 60 0С, об’єм газу 2,5 м3. Визначити об’єм газу для нормальних умов. Виходячи із рівняння
Р0 = 760 мм рт. ст. (0,101МПа). Рнад = 0,3 + 0,101 = 0,401 МПа.
Іноді технічні розрахунки спрощують, якщо тиск газу мало відрізняється від атмосферного: V0 = V Приклад 1-4. Суміш газів має об'ємний склад (%): СО2 - 12, N2 - 74, H2O - 6, О2 - 7, СО - 1. Тиск суміші 0,1 МПа (750 мм рт. ст) Визначити молекулярну масу, газову сталу, густину суміші при температурі 10000С і парціальний тиск окремих газів. 1) 2) 3) із рівняння стану для 1 кг газу Pv = RT, або 4) Рі = Р∙аі (тут аі - об'ємна частка газу) Р CO2 = 0.1∙0.12 = 0.012 МПа = 12 кПа, Р N2 = 0.1∙0.74 = 0.074 МПа = 74 кПа, Р Н2О = 0,1∙0,06 = 0,006 МПа = 6кПа, Р О2 = 0,1∙0,07 = 0,007 МПа = 7кПа, Р СО = 0,1∙0,01 = 0,001 МПа = 1 кПа. Приклад 1-5. Балон із киснем ємністю 20 л перебуває під тиском 10 МПа при 150С. Після витрати частини кисню тиск знизився до 7,6 МПа, а температура впала до 100С. Визначити масу витраченого кисню. Із характеристичного рівняння (1.2)
Витрати кисню склали 2,673 - 2,067 = 0,606 кг. Приклад 1-6. Посудина ємністю V = 10 м3 заповнена 25 кг СО2. Визначити абсолютний тиск в посудині, якщо t = 270C. Із характеристичного рівняння
Приклад 1-7. Атмосферне повітря має наступний масовий склад: mo2 = 23.2%, mN2 = 76.8%. Визначити об'ємний склад повітря, його газову сталу уявну молекулярну масу, парціальний тиск О2 і N2, якщо тиск повітря (барометричний) В = 101325 Па.
Уявна молекулярна маса Мсум = rO2 MO2 + rN2MN2 = 0.21∙32 + 0.79∙28.02 = 28.9, або
Парціальний тиск РО2 = rО2∙Р = 0,21∙101325 = 21278 Па, РN2 = rN2∙Р = 0,79∙101325 = 80047 Па. 1.3 Теплоємність газів. ЗмішуванняРозрізняють мольну теплоємність М∙С Масова теплоємність С' = С Середня теплоємність в межах t1... t2 дорівнює: Ст = q/ (t2 - t1), а дійсна (істинна) теплоємність
тут q - кількість тепла, переданого до одиниці кількості газу. Між мольною теплоємністю при Р = const і при V = const є зв’язок: МСР - МСV = МR = 8.314 кДж/ (кмоль*К), а СР /СV = К (для одноатомних газів К = 1,67; для двоатомних К = 1,4; для трьохатомних і багатоатомних К = 1,29). Залежність теплоємності від температури є нелінійною: C = a + bt + dt2, (1.3) де a, b, d - константи для кожного газу. В розрахунках часто нелінійну залежність заміняють близькою до неї лінійною: C = a + bt, а середня теплоємність при зміні температури від t1 до t2 складає:
В табл. .1.1 наведені формули для підрахунку середніх значень масової та об'ємної теплоємності газів за лінійним законом зміни температури. Таблиця 1.1 Середня масова та об'ємна теплоємність газів (лінійна залежність)
Приклад 1-8. Визначити середню теплоємність Сpm повітря при Р = const в межах 200...8000С, виходячи із нелінійної залежності теплоємності від температури. Кількість теплоти, яка передається від t1 до t2 складає: qp = Cpm2∙t2 - Cpm1∙t1, a
Табульовані значення теплоємності (табл. Д4, табл. ХІІ 4)
При змішуванні газів, які не реагують хімічно, мають різні температури та тиск, розрізняють 2 випадки: 1 - змішування при V = const (сумарний об’єм газів перед і після змішування). Параметри стану визначаються за формулами:
Для газів із однаковими мольними теплоємностями (та однаковими значеннями К).
2 - змішування газових потоків (масові витрати
Мі -
при температурі Т, тиску Р. Якщо гази перебувають під однаковим тиском, то
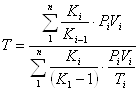
Приклад 1-9. У двох посудинах утримуються гази: посудина А - 50 л азоту, при Р1 = 2МПа, t1 = 2000С; посудина В - 200 л диоксиду вуглецю при Р2 = 0,5МПа, t2 = 6000С. Визначити тиск і температуру, які будуть встановлені після приєднання посудин. Значення
1.4 Аналітичний вираз І законуну термодинаміки має вигляд:dQ = dU + dL, де dQ - кількість теплоти, яку робоче тіло отримало зовні, dU - зміна внутрішньої енергії робочого тіла, dL - робота, яку здійснило робоче тіло ("зовнішня робота розширення"). Для нескінчено малої зміни стану робочого тіла dq = du + pdu = = d (u+ pu) - udp. I = u + pu є параметром стану, має назву ентальпії. Для ідеального газу
де Сpm - середня масова теплоємність при р = const в межах 0...Т. Для теплотехнічних розрахунків необхідно знати зміну ентальпії, а не її абсолютне значення. При р = const кількість теплоти qp = i2 - i1, тобто різниця ентальпій кінцевого і вихідного стану. Приклад 1-10. В котельній електростанції за 20 год. спалено 62т кам’яного вугілля, яке має теплоту згорання 28900 кДж/кг. Визначити середню потужність станції, якщо в електричну енергію перетворено 18% теплоти, отриманої від спалення вугілля. Кількість теплоти, яка перетворена в електричну енергію, складає: Q = 62*1000*28900*0,18кДж. Еквівалентна електрична енергія або робота
Страницы: 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 |
Copyright © 2012 г.
При использовании материалов - ссылка на сайт обязательна.
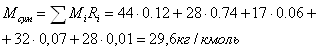
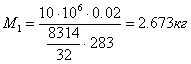 , а після витрат
, а після витрат 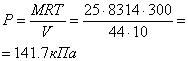
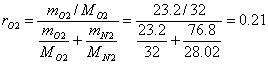
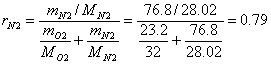
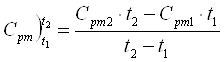
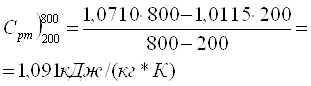
 (1.4)
(1.4) ,
, 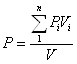 .
. (1.7)
(1.7) ,
, 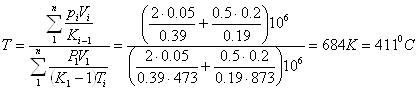
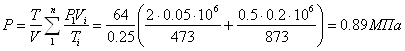 .
.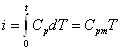 (1.9)
(1.9)