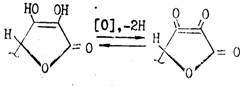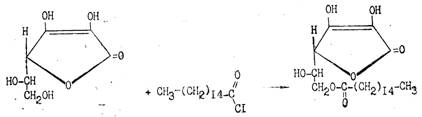|
|
МЕНЮ
|
Курсовая работа: Технология производства аскорбиновой кислоты (витамина С)Курсовая работа: Технология производства аскорбиновой кислоты (витамина С)Введение Аскорбиновая кислота впервые выделена в чистом виде Сцент-Гиорги в 1928 г. под названием гексуроновая кислота. В 1933 г. рядом исследователей установлена ее структура. Синтез ее осуществлен впервые Рейхштсйном в Швейцарии, Гевортом в Англии, Хеуорзом и Хирстом с сотр. также в Англии. Значение витамина С для организма человека очень велико. Аскорбиновая кислота принимает активное участие в окислнтельно-восстановительных процессах в организме и входит в состав ряда сложных ферментов, обусловливающих процессы клеточного дыхания. Витамин С участвует в процессах углеводного и белкового обмена, повышает сопротивляемость организма к инфекционным заболеваниям, регулирует холестериновый обмен, участвует в нормальном функционировании желудка, кишечника и поджелудочной железы; совместно с витамином Р обеспечивает нормальную эластичность стенок кровеносных капилляров, обезвреживает действие ряда лекарственных веществ и ядов. Аскорбиновая кислота применяется при лечении цинги, инфекционных заболеваний, ревматизма, туберкулеза, язвенной болезни, при гепатитах, шоковом состоянии и др. При недостаточности аскорбиновой кислоты развивается гиповитаминоз, в тяжелых случаях — авитаминоз (цинга, скорбут). При цинге наблюдается утомляемость, сухость кожи, расшатываются и выпадают зубы, наблюдаются боли в конечностях, снижается сопротивляемость к инфекциям. В конечном итоге, цинга приводит к летальному исходу. В терапевтических дозах аскорбиновая кислота хорошо переносится и побочных эффектов не вызывает. При введении в больших дозах и в течение длительного времени она может повреждать островковый аппарат поджелудочной железы и опосредованно почки. Аскорбиновая кислота содержится в значительных количествах в овощах, плодах, ягодах, хвое, шиповнике, в листьях черной смородины. Под влиянием высоких температур, кислорода, особенно в присутствии тяжелых металлов, витамин С легко разрушается. В организме человека и большинства животных аскорбиновая кислота не синтезируется. Примерная суточная доза составляет 50—100 мг. В то же время, в некоторых случаях (тяжелые физические нагрузки, простудные заболевания) показаны увеличенные (ударные) дозы аскорбиновой кислоты (до 0,5-1,0 г и более на прием). Активным пропагандистом этих воззрений является известный американский химик, лауреат Нобелевской премии Л. Полинг. Строение и физико-химические свойства аскорбиновой кислоты Строение аскорбиновой кислоты следующее:
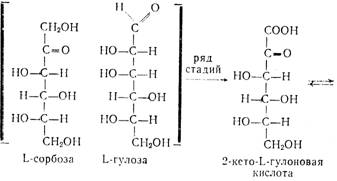
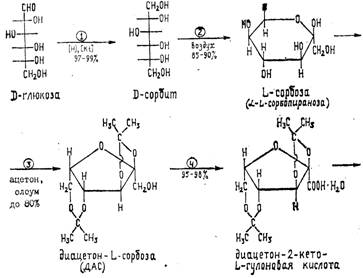
Аскорбиновая кислота является производным моносахарида L-ряда. Это строение подтверждено синтезами, в которых исходными веществами являются L-сорбоза (наиболее доступна) или L-гулоза, превращающиеся в 2-кето-Ь-гуло-новую кислоту—ключевой полупродукт в синтезе аскорбиновой кислоты:
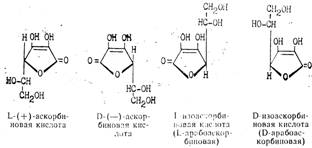
Аскорбиновая кислота имеет два асимметрических атома углерода в положениях 4 и 5 и образует четыре оптических изомера и два рацемата:
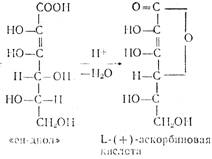
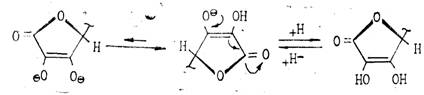
Биологически активной является L-(+)-форма. Д-(—)-форма является антивитамином и не существует в природе. Принятое строение аскорбиновой кислоты подтверждается рентгеноструктурным анализом. Молекулярная модель, установленная этим методом, показывает, что все атомы углерода и кислорода цикла лежат в одной плоскости, кроме С4, лежащего вне ее. Аскорбиновая кислота представляет собой белое кристаллическое вещество с Тпл 192°, очень чувствительна к нагреванию, хорошо растворима в воде, плохо в спиртах (за исключением метанола), практически нерастворима в неполярных растворителях. Она очень чувствительна к тяжелым металлам, медь и железо разрушающе, действуют на аскорбиновую кислоту. Аскорбиновая кислота легко отщепляет протон гидроксила в положении Сз кольца и по силе не уступает карбоновым кислотам:
Аскорбиновая кислота является двухосновной, однако, ее считают практически одноосновной, поскольку pKI=4 12 а рКII =11,57. Кислотность обусловлена фенольной НО-группой. Аскорбиновая кислота легко образует соли — наиболее известна ее натриевая соль (аскорбинат натрия). Аскорбиновая кислота очень легко окисляется и обладает сильной восстановительной способностью. Процесс окисления аскорбиновой кислоты протекает сложно, начальной стадией его является образование т. н. дегидроаскорбиновой кислоты под влиянием кислорода воздуха или других окислителей. Этот процесс является обратимым:
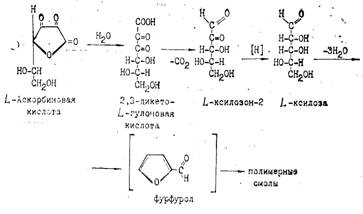
При рН<7 в процессе окислительного и гидролитического расщепления дегидроаскорбиновая кислота, например, превращается в 2,3-дикето-L-гулоновую кислоту. Последняя под влиянием повышенной температуры декарбоксилируется и превращается в L-ксилозон-2. Ксилозон восстанавливается аскорбиновой кислотой в L-ксилозу, которая циклизуется в фурфурол путем дегидратации:
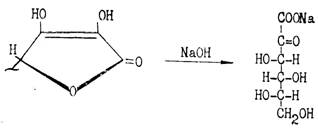
Известно, что фурфурол легко вступает в реакции присоединения, образуя полимеры, а также легко окисляется с раскрытием цикла и образованием янтарной и других органических кислот и смолистых веществ. Указанные процессы протекают даже в присутствии кислорода воздуха, образуя цикл каталитического разложения аскорбиновой кислоты. Поэтому желательно исключить воздействие кислорода на растворы аскорбиновой кислоты и ее препараты в производстве и при хранении. Естественно, что в присутствии более сильных окислителей и, особенно, ионов тяжелых металлов (медь, магний, железо) аскорбиновая кислота окисляется с деструкцией цикла и образованием в итоге различных органических кислот (L-трео-новая, глицериновая, щавелевая и др.). Все процессы окисления идут легче в щелочной среде. При нагревании со щелочами аскорбиновая кислота легко гидролизуется, превращаясь в соль 2-кето-L-гулоновой кислоты:
Из других свойств аскорбиновой кислоты следует отметить ее способность к образованию простых и сложных эфиров. Наиболее известен пальмитат аскорбиновой кислоты, который используют для витаминизации пищевых продуктов:
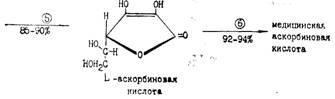
Методы синтеза аскорбиновой кислоты, выбор рационального способа производства Аскорбиновая кислота может быть получена из моносахаридов D- или L-ряда. Известно несколько методов ее синтеза. 1. Бензоиновый метод. В основе лежит конденсация— треозы и этилглиокислота в присутствии KCN. Метод неперспективен из-за дефицитности сырья, низкого выхода. 2. Циангидриновый метод. Аскорбиновую кислоту получают, исходя из L-ликсозы или L-ксилозы. Практического применения не имеет из-за отсутствия сырья, синтез которого из D-глюкозы очень сложен. 3. Получение аскорбиновой кислоты из свекловичного «жома» (отходы производства сахара из свеклы). Метод предложен американцами в 1904 г. Метод нуждается в значительном усовершенствовании: из 100 кг жома получают всего 2,5 кг аскорбиновой кислоты. 4. Частично микробиологический метод получения аскорбиновой кислоты из D-глюкозы. Включает 5 стадий, в т. ч. 3 химических. В основе метода лежит окисление D-глюкозы уксуснокислыми бактериями до кальциевой соли 5-кето-0-глюконовой кислоты, которую превращают в L-аскорбиновую кислоту. Метод привлекает внимание ограниченным применением химических реагентов. Однако выход продукта низок, а процессы микробиологического синтеза трудно управляемы. 5. Метод Рейхштейиа. Синтез L-аскорбиновой кислоты из 2-кето-L-гексоновой кислоты. Основное сырье (D-глюкоза) и вспомогательные реагенты, применяемые для синтеза, используются в пищевой и химической промышленности. Метод нашел применение во многих странах, в т. ч. СССР. Усовершенствован во ВНИХФИ, в настоящее время отдельные стадии его совершенствуются в НПО «Витамины». Метод Рейхштейна состоит из 6 стадий, включая 1 стадию микробного синтеза: 1 стадия. Получение D-сорбbта из D-глюкозы методом каталитического восстановления водородом. 2 стадия. Получение L-сорбозы из D-сорбита путем его глубинного аэробного окисления уксуснокислыми бактериями. 3 стадия. Получение диацетон-L-сорбозы из L-сорбозы путем ее ацетонирования. 4 стадия. Получение гидрата диацетон-2-кето-L-гулоновой кислоты путем окисления диацетон-L-сорбозы. 5 стадия. Получение L-аскорбиновой кислоты из гидрата диацетон-2-кето-L-гулоновой кислоты (деацетонирование —> этерификация —> «енолизация» —> «лактонизация»). 6 стадия. Получение медицинской аскорбиновой кислоты. Перекристаллизация технической аскорбиновой кислоты. Выход продукта в пересчете па глюкозу составляет в целом до 54%. Химическая схема производства аскорбиновой кислоты
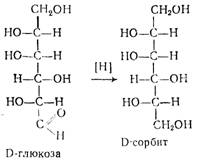
Технология производства аскорбиновой кислоты Стадия 1. Производство D-сорбита из D-глюкозы В производстве синтетической аскорбиновой кислоты D-сорбит является первым промежуточным продуктом синтеза. D-сорбит представляет собой белый кристаллический порошок, легко растворимый в воде. Сырьем для его производства является D-глюкоза. Это сравнительно дорогое сырье, стоимость его составляет 40—44% от себестоимости аскорбиновой кислоты, поэтому замена D-глюкозы на непищевые виды сырья является важной проблемой. Процесс восстановления D-глюкозы можно осуществлять двумя методами: — электролитическим восстановлением; — каталитическим гидрированием. Электролитическое восстановление D-глюкозы в D-сорбит осуществляется при комнатной температуре в электролизерах со свинцовыми анодами и катодами из сплава никеля. Процесс проводят в присутствии NaOH и сульфата натрия или аммония при рН=10. Преимущество процесса заключается в мягких условиях его проведения, в отсутствии дорогостоящих катализаторов и автоклавов. Однако в процессе электролитического восстановления получается раствор D-сорбита, загрязненный его изомером—D-маннитом (до 15%). Разделение этих изомеров представляет большие трудности. Недостатком процесса является также высокая щелочность раствора и сложность конструкции электролизера. Поэтому в настоящее время на витаминных предприятиях принят каталитический метод. Каталитическое гидрирование (восстановление) можно представить следующей схемой:
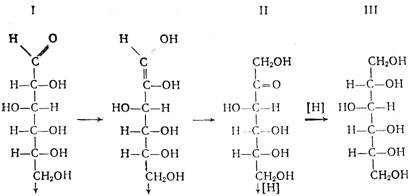
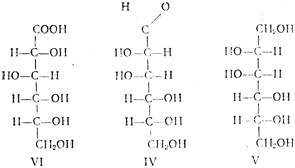
Выход составляет 98—99% от теоретически возможного. Особенностью этой стадии производства является протекание ряда побочных реакций: окисление D-глюкозы (I) в D-глюконовую кислоту (VI) кислородом воздуха в присутствии катализатора; фенолизация D-глюкозы в щелочной среде с последующей изомеризацией в D-фруктозу (II) и D-маннозу (IV). D-фруктоза может далее превращаться в D-сорбит (III) и D-маннит (V). В побочных процессах гидрогенолиза глюкозы, кроме D-сорбита, образуются также этиленгликоль, глицерин, пропиленгликоль и др. побочные продукты. Основные побочные процессы протекают по схеме:
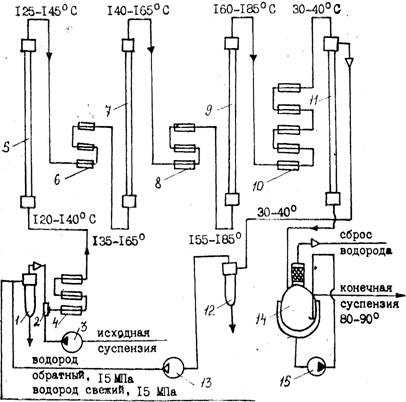
Основная задача при осуществлении технологического процесса—свести к минимуму образование этих побочных продуктов. Это достигается рядом мер, которые будут рассмотрены несколько позже. Технологическая схема получения D-сорбита включает следующие операции: 1) Приготовление и регенерация скелетного никелевого катализатора. 2) Приготовление 50—55%-ного раствора D-глюкозы. 3) Получение D-сорбита. 4) Очистка водного раствора D-сорбита от ионов тяжелых металлов. 5) Получение кристаллического D-сорбита для выпуска пищевого D-сорбита. Процесс гидрирования глюкозы осуществляют двумя способами: или автоклавным периодическим способом, или в непрерывно действующих аппаратах. Периодический способ Процесс приготовления и регенерации никелевого катализатора из сплава Ni—Al изучался ранее в других курсах, поэтому в предлагаемом тексте лекций не рассматривается. Для гидрирования приготавливают 50—55%-ный водный раствор D-глюкозы при 70—75°С, очищают раствор активированным углем при 75 °С, фильтруют через нутч-фильтр. В очищенный раствор добавляют известковую воду до рН 8,0—8,1 и раствор направляют на гидрирование. В настоящее время разработан способ непрерывной очистки 50%-ных растворов глюкозы на гранулированном угле АГ-3. Расход его значительно меньше, чем порошкообразного, он легче регенерируется. Наряду с этим проводятся исследования по очистке 50%-ных водных растворов глюкозы с использованием полимерных мембран и ионообменных смол. Автоклавный процесс гидрирования осуществляют при температуре 135—140°С, и рН=7,5—7,8 под давлением 70— 100 атм. при непрерывной подаче водорода, полученного электролитическим путем, в автоклав. Окончание процесса определяют по прекращению падения давления водорода в автоклаве в течение 20 мин. Раствор сорбита охлаждают до 75— 80 °С, снижают давление в автоклаве до 5—7 атм. и направляют раствор сорбита совместно с катализатором на фильтрацию. Катализатор отделяют на друк-фильтре и тщательно отмывают горячей водой. Затем катализатор направляют на регенерацию. Как уже указывалось, процесс гидрирования сопровождается рядом побочных реакций. Для того, чтобы свести их к минимуму, необходимо в периодическом процессе: — не допускать хранения щелочного раствора D-глюкозы с катализатором; — проводить реакцию гидрирования при рН, близком к нейтральному (7,3—7,5), т. к. в щелочной среде D-глюкоза будет подвергаться распаду при t==135—140°С. Однако при смешении катализатора с раствором D-глюкозы в автоклаве наблюдается некоторое снижение величины рН, поэтому рН раствора в начале процесса следует доводить до 8,0, а раствор глюкозы готовить на дистиллированной воде (он должен быть прозрачным и не содержать посторонних солей). Следует использовать особо чистый, электролитический водород. Катализатор необходимо тщательно подготовить и промыть. Величина зерен катализатора—1—2 мм. Остаточное содержание глюкозы по окончании гидрирования не должно превышать 0,1% по массе. Непрерывный способ Па предприятиях Венгрии, Германии, некоторых американских фирм, в России (г. Йошкар-Ола) процесс гидрирования глюкозы в сорбит ведут непрерывным способом. При непрерывном способе более эффективным является применение суспензированного катализатора, т. к. при этом достигается повышение контактной поверхности катализатоpa и наилучшее использование объема автоклава. На основе венгерской лицензионной технологии процесс гидрирования в Йошкар-Оле (рис. 1) осуществляют в каскаде из колонных автоклавов при температуре 140—165°С и давлении 150 атм.
Рис. 1. Схема узла гидрирования D-глюкозы непрерывным способом: 1 - маслоотделитель; 2 — смеситель; 3-—насос высокого давления; 4, 6. 8 — пароподогреватели высокого давления; 5, 7, 9 - - реакторы высокого давления: 10 — холодильник высокого давления; 11—сепаратор высокого давления; 12 — брызугоуловитель высокого давления; 13 — циркуляционный компрессор; 14 — сепаратор с брызгоуловителем; 15 — циркуляционный насос Предварительно готовят 50%-ный раствор глюкозы при t=80°С, охлаждают его до 30—40 °С и подают на гидрирование через специальный смеситель с катализатором. В системе смесителей готовят 10%-ную суспензию никелевого катализатора в известковой или аммиачной воде, смешивают ее с 50%-ным раствором глюкозы и насосами-дозаторами направляют в три последовательно соединенные колонны. Водород подается в тот же смеситель. По окончании процесса гидрирования раствор сорбита совместно с катализатором поступает для сепарации водорода в сборник, а затем на фильтрацию (система сепаратор—фильтр). Отработанный катализатор промывают горячей водой и передают на регенерацию, а раствор D-сорбита — на очистку. В настоящее время проведены испытания более технологичного и простого процесса гидрирования на стационарном никелевом катализаторе. Медно-никелевый стационарный катализатор применяют в ГДР для гидрирования глюкозы при t=120—140°С и избыточном давлении 201—240 кгс/см2.Непрерывный процесс гидрирования позволяет применять автоматические контроль и регулирование, обеспечивать более высокое качество продукта и увеличивать производительность труда. Очистка сорбитного раствора Очистка производится двумя способами: 1) химическим — методом осаждения ионов тяжелых металлов (меди, железа, никеля) с помощью двузамещенного фосфорнокислого натрия (Na2HPО4) имела. К 20—25%-ному раствору сорбита добавляют 1,5—2% Na2HP04 и 2—S% мела (к массе раствора), нагревают d течение 1 ч до 85— 90 °С, фильтруют через нутч-фильтр или фильтр-пресс с применением асбестовой или угольной подушки. По окончании фильтрации раствор сорбита подвергают анализу. 2) на ионообменных смолах — 25—30%-ный раствор сорбита пропускают через две колонны, заполненные катионитом (Н-+-форма) 1\У-2. При этом рН раствора значительно снижается за счет ионного обмена. Для повышения рН до 4,0— 4,6 раствор пропускают через 3 непрерывно действующие колонны, заполненные слабоосновным анионитом ЭДЭ-10П. Для получения кристаллического продукта очищенный раствор сорбита выпаривают в вакуум-аппарате при вакууме не ниже 650 мм рт. ст. до содержания сухих веществ 70— 80%. Часть раствора сорбита упаривают на РПИ до содержания влаги 5% и кристаллизуют. Кристаллы отфильтровывают, промывают спиртом и высушивают при температуре 35—40 °С. Получают чистый медицинский сорбит, используемый для лечебных и пищевых целей. Гранулированный D-сорбит из водного концентрата производят на специальной сушильной установке. Стадия 2. Производство L-сорбозы из D-сорбита
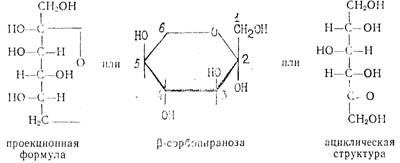
L-сорбоза является кетогексозсй, в кристаллическом виде имеет р-форму пиранозы. Хорошо растворима в воде, плохо в спирте, Тпл= 165°С. Строение L-сорбозы можно представить различными структурами- Страницы: 1, 2 |
|||||||||||||||||||||||||||||||||||||||||
Copyright © 2012 г.
При использовании материалов - ссылка на сайт обязательна.