ГЛАВА 22. ОБСЛЕДОВАНИЕ ПАЦИЕНТОВ
С ОБЪЕМНЫМИ ОБРАЗОВАНИЯМИ ПЕЧЕНИ
1. С чего следует начинать
обследование пациентов с объемными образованиями печени?
Первый шаг — тщательный сбор
анамнеза и объективное обследование. Возраст, пол, место рождения могут
помочь в определении этиологии заболевания. Имеющиеся в анамнезе факторы
риска развития вирусного гепатита или цирроз печени повышают вероятность
обнаружения первичной злокачественной опухоли. Наличие у пациента новообразований
других органов позволяет заподозрить метастатическую болезнь. Необходимо
отметить факт использования пероральных контрацептивов или анаболических
стероидных гормонов, злоупотребления алкоголем, а также потенциальную возможность
контакта с канцерогенными веществами (винилхлорид). У больного нередко
выявляются гепатомегалия и/или спленомегалия, болезненность печени при
пальпации или знаки хронического заболевания печени (гиперемия ладоней
или сосудистые звездочки).
Лабораторные тесты, за исключением
уровня а-фетопротеина в сыворотке, неспецифичны и не сужают диагностический
поиск. Определение уровня печеночных ферментов, альбумина и серологических
маркеров гепатита В и С, коагулограмма, а также оценка метаболизма железа
помогают предположить наличие у больного фонового заболевания печени —
хронического гепатита, цирроза или инфильтративного процесса.
Дифференциальная диагностика объемных
образований печени у взрослых
|
ДОБРОКАЧЕСТВЕННЫЕ
|
ЗЛОКАЧЕСТВЕННЫЕ
|
|
|
Эпителиальные
опухоли
|
|
|
|
Аденома печени
Аденома желчного протока Билиарная цистаденома
|
Гепатоцеллюлярная
карцинома Холангиокарцинома Билиарная цистаденокарцинома Плоскоклеточная
карцинома
|
|
|
Мезенхимальные
опухоли Кавернозная гемангиома
|
Ангиосаркома
Эпителиоидная гемангиоэндотелиома
|
|
|
Фиброма Лейомиома
Липома
|
Фибросаркома
Лейомиосаркома Липосаркома Рабдомиосаркома Первичная лимфома печени
|
|
|
Прочие заболевания
Местная узелковая гиперплазия Абсцесс печени Крупноузловой цирроз печени
Местная жировая инфильтрация Фокальный участок сохраненной паренхимы на
фоне диффузной жировой инфильтрации Простые печеночные кисты Микрогамартома
(комплекс ван Мейенбурга [von Meyenburg])
|
|
|
2. Какие доброкачественные
заболевания чаще всего дают картину объемного образования печени?
Кавернозные гемангиомы —
наиболее распространенные доброкачественные опухоли печени, встречающиеся
у 1-20 % населения. Они развиваются у людей любого возраста, чаще у женщин.
Кавернозная гемангиома представляет собой единичное объемное образование
размером менее 3 см, расположенное обычно в заднем сегменте правой доли
печени; течение заболевания, как правило, бессимптомное. Термином гигантская
гемангиома некоторые авторы определяют опухоли, размеры которых превышают
4 см. Как показывает микроскопическое исследование, гемангиома состоит
из заполненных кровью синусоидов, разделенных соединительно-тканными перегородками.
Изредка рост гемангиомы провоцируется беременностью или приемом эстрогенных
препаратов. Иногда размеры опухоли настолько велики, что вызывают боли
в животе, однако риск ее спонтанного разрыва незначителен. Поэтому хирургическое
удаление гемангиомы не оправдано, за исключением тех случаев, когда клинические
симптомы ярко выражены. Лечение гемангиомы рентгенотерапией или эмболизацией
не всегда успешно.
3. Как можно обнаружить
гемангиому печени?
Гемангиома нередко обнаруживается
случайно при ультразвуковом сканировании (УЗИ) органов брюшной полости
или компьютерной томографии (КТ). Ультразвуковые признаки гемангиомы различны,
но чаще всего она представляет собой однородное гиперэхогенное образование
с четкими границами, дающее акустическую дорожку. Такая ультразвуковая
картина характерна также для многих других доброкачественных и злокачественных
новообразований печени и требует проведения дальнейших исследований.
При размере новообразования
2,5 см в диаметре и более методом выбора является эмиссионная компьютерная
томография одиночных фотонов (SPECT) с использованием эритроцитов,
меченных технецием 99т. Медленный ток крови, поступающей из нормальных
артериальных сосудов, через каверны гемангиомы приводит к тому, что она
скапливается в этом своеобразном депо. Происходит аккумуляция меченых эритроцитов,
а на отсроченных снимках (выполненных через 1-2 ч) выявляется повышение
радиоактивности в данной зоне. SPECT подтверждает диагноз гемангиомы, т.
к. обладает 100 % специфичностью. Однако он не всегда определяет гемангиомы
маленького размера, тромбированные, облитерированные или расположенные
вблизи основных внутрипеченочных сосудов. Поэтому чувствительность данного
метода в целом ниже и составляет 80-90 %.
Магнитно-резонансная
томография (МРТ) применяется при подозрении на гемангиому размером
менее 2,5 см. На томограммах гемангиома выглядит как образование пониженной
или нормальной плотности, однако ее изображение становится значительно
более) плотным (ярким) на томограммах (симптом "электрической лампочки").
Наличие гиперваскуляризированных метастазов эндокринных опухолей, аденокарциномы
или саркомы иногда приводит к ложноположительным результатам.
Метод последовательного
динамического болюсного компьютерного сканирования является диагностически
ценным, если: (1) плотность образования невелика на неусиленных томограммах;
(2) в динамической болюсной фазе отмечается усиление периферического контрастирования;
(3) образование становится нормальной или повышенной плотности на отсроченных
сканограммах. Лишь 55-62 % всех гемангиом удовлетворяют этим условиям.
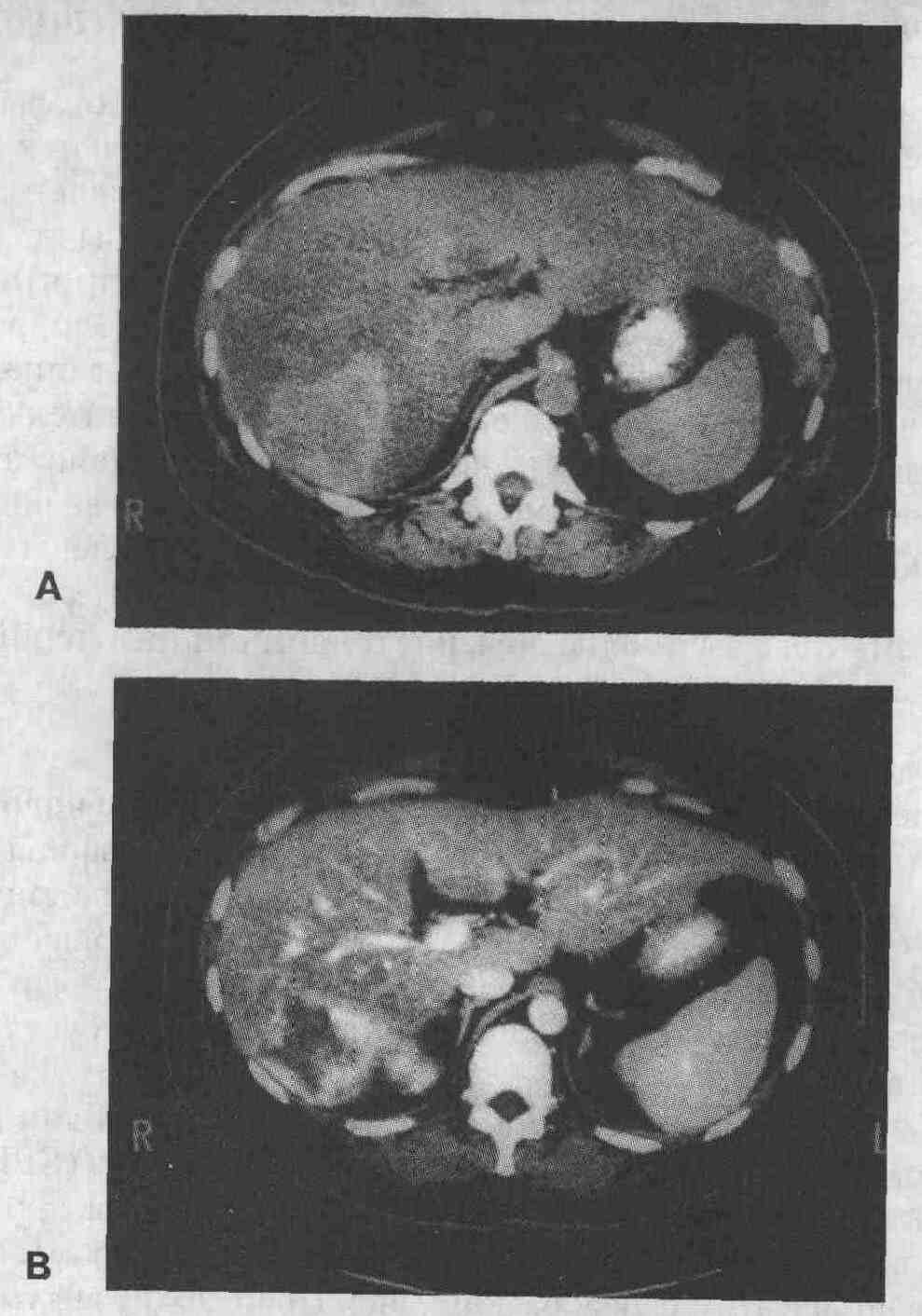
Неусиленное (А) и усиленное (В) компьютерное
изображение гемангиомы в правой доле печени
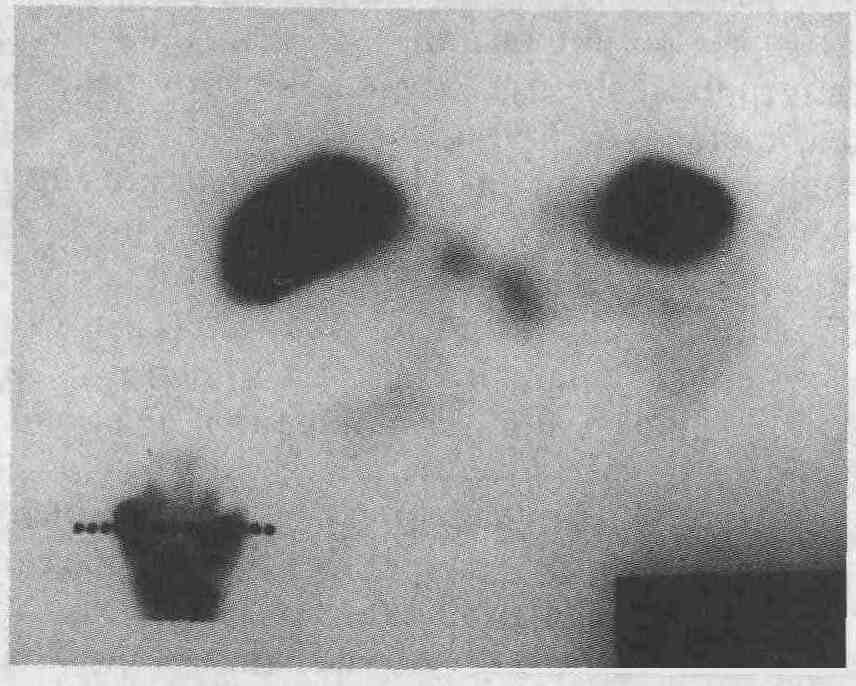
Отсроченный SPECT-снимок того же образования
подтверждает диагноз гемангиомы. Обратите внимание на скопление радиоактивных
эритроцитов
Поскольку в распоряжении
врача имеются точные неинвазивные методы исследования, ангиография применяется
редко. На ангиограммах определяется быстрое конт-растирование гемангиомы
в артериальной фазе и стойкое, сохраняющееся контрас-тирование в венозной
фазе; образование новых кровеносных сосудов и артерио-венозные шунты отсутствуют.
Чрескожная биопсия опухоли,
пропагандируемая
некоторыми клиницистами, принята в качестве метода окончательной диагностики
далеко не всеми. Более разумным подходом при прочих равных условиях является
повторное выполнение КТ или МРТ через 2-3 месяца для подтверждения отсутствия
изменений в найденном образовании.
4. Почему факт использования пероральных
контрацептивов имеет такое большое значение для проведения дифференциальной
диагностики при объемных новообразованиях печени?
В большинстве случаев развитие
аденом печени непосредственно связано с применением пероральных контрацептивов.
Эти доброкачественные опухоли печени редко обнаруживались до тех пор, пока
в 1960-х гг. пероральные противозачаточные средства не стали доступны широким
слоям населения. У женщин риск образования аденом печени зависит от длительности
приема контрацептивов; у большинства пациенток таковая составляет 4-5 лет.
С возрастом (старше 30 лет) риск возникновения заболевания повышается.
Уменьшение активности эстрогенового компонента контрацептивов может снизить
заболеваемость, которая в 1970-е гг. составляла 3-4 человека на 100 000.
У мужчин аденомы печени встречаются редко, хотя описаны случаи их обнаружения
при назначении анаболических стероидных гормонов. Аденомы печени диагностируются
преимущественно у молодых женщин и женщин среднего возраста и протекают
бессимптомно. При объективном обследовании определяется увеличение печени
или пальпируемое новообразование. Примерно 25 % больных предъявляют жалобы
на боль в животе, возникающую в результате кровоизлияния в опухоль с последующим
ее некрозом. В 30 % случаев (особенно во время менструаций, беременности
или в послеродовом периоде) вероятен спонтанный разрыв опухоли с развитием
гемоперитонеума. При потенциальной возможности разрыва и образовании в
аденоме документально подтвержденного гепатоцеллюлярного рака больному
показана резекция печени в пределах здоровых тканей. Известно, что аденомы
печени регрессируют или исчезают после отмены противозачаточных препаратов,
однако этот факт не должен определять тактику выбора.
5. Каковы гистологические характеристики
аденомы печени? Как выглядит опухоль при ультразвуковом и компьютерном
сканировании и МРТ?
Аденома печени — это опухоль,
имеющая четкие контуры, мясистую консистенцию и хорошо выраженный поверхностный
сосудистый рисунок. В большинстве случаев диаметр аденомы равен 8-15 см.
Микроскопически она состоит из пластов гепатоци-тов нормального или маленького
размера, между которыми отсутствуют желчные протоки, портальные дольки
и центральные вены. Фиброзные перегородки и клетки Купфера визуализировать
не удается.
Внешние признаки аденомы
печени достаточно вариабельны: от гипо- до гиперэхоген-ных образований
при ультразвуковом сканировании и от гипо- (пониженной плотности) до гиперденсивных
(повышенной плотности) образований при КТ. На компьютерных томограммах,
особенно по периферии новообразования, может отмечаться усиление контрастности
изображения. Повышенная плотность центральных участков опухоли, представленных
очагами кровоизлиянии, свидетельствует в пользу предполагаемого диагноза.
МРТ характеризуется такой же степенью вариабельности и является неспецифичным
методом исследования.
6. Каково значение сканирования
печени с коллоидной серой, меченной Те99m, в диагностике
объемных образований?
Большинство доброкачественных
и злокачественных новообразований печени определяются на сканограммах в
виде дефектов наполнения. Это происходит из-за того, что радиоактивная
сера захватывается клетками Купфера, а следовательно, нормальное изображение
можно получить только при неизмененной архитектонике печени. Исключение
из правил — местная узелковая гиперплазия. Полагают, что эта редкая доброкачественная
опухоль образуется вследствие порока развития артерий печени. Местная узелковая
гиперплазия (МУГ) — это округлое, некапсулированное образование, в центре
которого определяются рубцовая ткань, кровеносные сосуды, желчные протоки
и клетки хронического воспаления. От рубца, наподобие спиц в колесе, ради-ально
расходятся фиброзные перегородки, имеющие аналогичное гистологическое строение.
Находящиеся между перегородками гепатоциты расположены в виде узелков или
тяжей, так что микроскопическая картина напоминает таковую при циррозе
печени. Купферовские клетки, локализованные в пределах МУГ, поглощают коллоидную
серу, поэтому на сканограммах образование определяется как участок нормального
или избыточного поглощения по сравнению с окружающей здоровой тканью печени.
К сожалению, только 60-70 % МУГ содержат достаточное количество купферовских
клеток, чтобы картина при сцинтиграфии соответствовала описанной. В остальных
случаях МУГ выявляется в виде холодного дефекта наполнения, который требует
проведения дальнейших исследований.
7. Каковы клинические
и прогностические различия между местной узелковой гиперплазией и аденомой
печени?
Так же как и аденома печени,
местная узелковая гиперплазия развивается преимущественно у женщин и диагностируется
в возрасте от 20 до 60 лет. МУГ обычно имеет меньшие размеры (часто <
3 см) и протекает в основном бессимптомно. В отличие от аденомы, МУГ не
является источником кровотечения, не склонна к разрывам или ма-лигнизации.
Несмотря на предположения, что эстрогены способны ускорять рост МУГ, пероральные
контрацептивы не относят к причинам возникновения этой опухоли. Хирургическое
лечение больным с местной узелковой гиперплазией не показано.
8. Какие еще внешние признаки
характерны для местной узелковой гиперплазии?
УЗИ и КТ не позволяют дифференцировать
МУГ от других новообразований печени. Как правило, на неусиленных компьютерных
томограммах МУГ обнаруживается в виде гиподенсивного образования, хотя
опухоль иногда имеет плотность, одинаковую с плотностью печени, и сливается
с окружающей тканью. Дополнительное конт-растирование приводит к появлению
сигнала различной интенсивности, а центральный рубец при УЗИ или КТ может
и вовсе не определяться. В подобных ситуациях МРТ оказывается более результативным
методом. Согласно недавно полученным данным, МРТ подтверждает диагноз МУГ,
если: (1) при сканировании в режиме Т1 и Т2 опухоль выявляется в виде гомогенного
изоинтенсивного образования; (2) интенсивность сигнала во время исследования
не изменяется; (3) центральный рубец дает гиперинтенсивное изображение
(на Т2-томограммах). К сожалению, такая характерная картина встречается
менее чем у половины пациентов, и дальнейшее исследование требует выполнения
ангиографии или клиновидной биопсии печени.
9. Возможно ли формирование
центральных рубцов при других объемных образованиях печени (кроме МУГ)?
Да Хотя центральные рубцы
наблюдаются преимущественно при МУ1, они могут формироваться также при
фиброламеллярном варианте гепатоцеллюлярного рака, гемангиомах и аденомах
печени. При МРТ центральный рубец доброкачественных образований (таких
как МУГ) характеризуется гиперинтенсивностью за счет сосудистого компонента
(при сканировании в режиме Т2). Злокачественные новообразования вследствие
фиброзных изменений имеют гипоинтенсивный рубец.
10. Какая злокачественная
опухоль печени встречается наиболее часто?
В США и странах Европы метастатическая
болезнь встречается значительно чаще, чем первично-злокачественные опухоли
печени. В основном метастазы в печень дают рак ободочной кишки, желудка,
поджелудочной железы, молочной железы и легких. Источником метастазов могут
также служить опухоли пищевода, почек и органов мо-' чеполовой системы.
Множественность очагов поражения предполагает наличие метастатического
процесса; частота обнаружения одиночных метастазов в печени составляет
лишь 2 %. Обычно в патологический процесс вовлекаются обе доли: 20 % случаев
приходится на правую долю и 3 % — на левую.
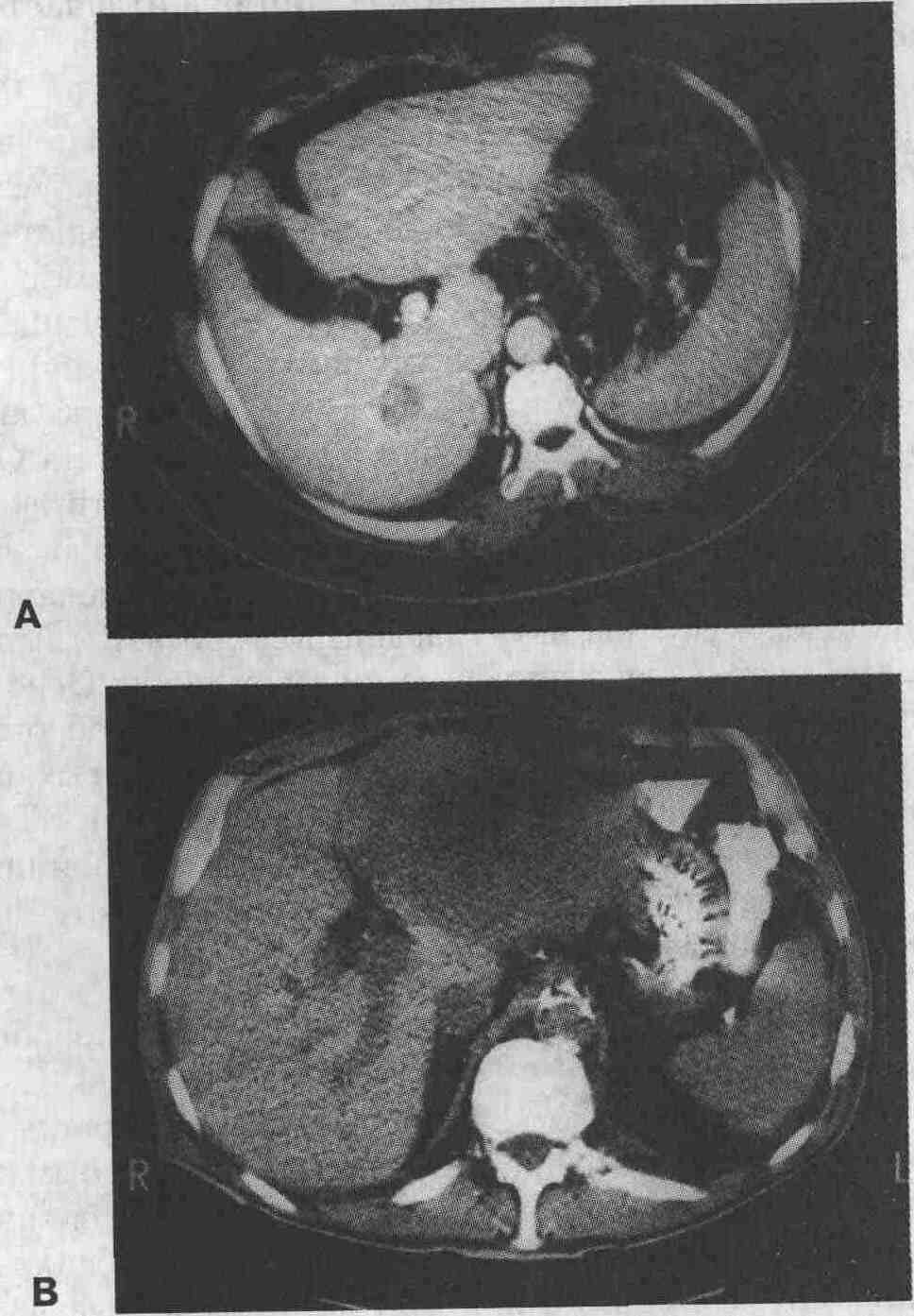
Различные КТ-проявления гепатоцеллюлярного
рака. А (с контрастированием). В правой доле определяется единичный узел
низкой плотности с усилением сигнала по периферии. В (без контрас-тирования).
Массивная форма роста рака со смещением левой доли
В странах Азии и Африки по
причине высокой распространенности вирусного гепатита В из злокачественных
опухолей печени преобладает гепатоцеллюлярный рак. Обычно (хотя не в 100
% случаев) он возникает на фоне длительно существующего цирроза печени.
В зависимости от характера роста он подразделяется на нодуляр-ный, местный
и диффузный. Нодулярная форма обнаруживается чаще всего и характеризуется
наличием одного или нескольких очагов поражения, локализованных в различных
сегментах печени. Местная форма рака развивается преимущественно у лиц
молодого возраста и представляет собой крупное единичное образование в
правой доле, часто окруженное мелкими сателлитными узелками. Диффузный
вариант рака встречается редко; он плохо определяется при визуализирующих
методах исследования, т. к. мелкие опухолевые очаги, поражающие большие
участки печени, очень похожи на цирротические узелки.
11. Что такое гепатобилиарная
цистаденома? Чем она отличается от доброкачественной кисты печени?
Простые кисты печени — достаточно
распространенная патология. Частота заболеваемости простыми кистами печени
составляет 2,5 %. Течение, как правило, бессимптомное. При УЗИ простые
кисты печени визуализируются в виде округлых образований с ровными контурами
и анэхогенным однородным содержимым; стенки отсутствуют. Если размер кисты
менее 2 см, она с трудом выявляется при компьютерной томографии. Подтвердить
диагноз позволяет в данном случае УЗИ печени. Гепатобилиарная цистаденома
отличается от доброкачественных кист печени наличием толстых стенок с многочисленными
выростами (септами). Однако многокамерные кисты встречаются чрезвычайно
редко, преимущественно у женщин среднего возраста. Они часто являются причиной
боли в животе. Гепатобилиарные цистаденомы достигают нескольких сантиметров
в диаметре и содержат слизь. Большинство из них доброкачественные; однако
25 % цистаденом малигнизируются (перерастают в цистаденокарциномы). Образование
в стенках цистаденомы узлов, выступающих в ее просвет, и выраженная кальци-фикация
свидетельствуют о злокачественном перерождении. Основной метод лечения
гепатобилиарной цистаденомы, даже если она протекает доброкачественно,—
хирургический (полное иссечение опухоли). Следует помнить, что выживаемость
при развитии цистаденокарциномы значительно снижается. При УЗИ, КТ и МРТ
абсцессы печени и эхинококковые кисты дают картину, сходную с таковой при
гепатобилиарной цистаденоме; дифференциальный диагноз при этом проводится
на основании клинической и серологической картины.
12. Цирроз печени какой
этиологии в наибольшей степени способствует развитию гепатоцеллюлярного
рака?
Результаты аутопсий показывают,
что 20-40 % больных, умерших от цирроза печени, имели рак печени, а у 56-84
% пациентов с диагностированным гепатоцеллюляр-ным раком обнаруживается
цирроз печени. Рак печени чаще всего возникает на фоне цирроза печени,
причиной которого стал гепатит В или С, особенно при наличии активной репликации
вируса. С образованием опухоли также связаны гемохроматоз и алкогольный
цирроз (в меньшей степени). Злоупотребление алкоголем может способствовать
развитию вирусного гепатита, а следовательно, и злокачественных ново-ббразрваний
печени.
Географический фактор влияет
как на возрастной показатель (в США пик заболеваемости отмечается у лиц
старше 55 лет), так и на соотношение полов (хотя в мировом масштабе у мужчин
гепатоцеллюлярный рак обнаруживается в 4 раза чаще, чем у женщин).
13. Перечислите некоторые
клинические и лабораторные признаки, позволяющие заподозрить наличие у
пациента гепатоцеллюлярного рака.
1. Появление болей в животе
или снижение массы тела у пациента с циррозом печени.
2. Гепатомегалия.
3. Аускультативный шум над
печенью.
4. Острое развитие гемоперитонеума.
5. Асцитическая жидкость,
окрашенная кровью.
6. Постоянная лихорадка.
7. Внезапное повышение уровня
щелочной фосфатазы в сыворотке крови.
8. Повышенное соотношение
ACT : АЛТ.
9. Эритроцитоз или стойкий
лейкоцитоз.
10. Гипогликемия.
11. Гиперхолестеринемия.
12. Гиперкальциемия.
Показатели с 9 по 12 относятся
к паранеопластическому синдрому, связанному с ге-патоцеллюлярным раком.
14. Какой уровень сывороточного
ос-фетопротеина обладает диагностической ценностью при гепатоцеллюлярном
раке?
а-Фетопротеин (АФП) — лучший
диагностический маркер гепатоцеллюлярного рака; он используется также при
скрининговом обследовании пациентов, относящихся к группе риска. Чувствительность
метода варьирует в зависимости от типа применяемого анализа; наибольшей
чувствительностью обладает радиоиммунный метод. Уровень АФП более 400 нг/мл
указывает на наличие гепатоцеллюлярной карциномы. Доброкачественные хронические
заболевания печени могут стать причиной неспецифического увеличения уровня
АФП, который практически никогда не превосходит указанное выше значение.
Уровень АФП коррелируется с размером опухоли; в случае успешного лечения
он может снизиться или даже нормализоваться. Не все гепатомы выделяют АФП.
Примерно у 30 % пациентов с гепатоцеллюлярным раком выявляется нормальный
уровень а-фетопротеина в сыворотке, особенно если размеры опухоли меньше
2 см (что позволяет выполнить ее резекцию). Пациентам с циррозом печени,
которые наиболее подвержены риску развития гепатоцеллюлярного рака, каждые
3-12 месяцев показано проведение скринингового обследования. Оно заключается
в определении уровня АФП в сыворотке крови и выполнении ультразвукового
сканирования печени. УЗИ с высокой разрешающей способностью — более чувствительный
метод ранней диагностики гепатомы, чем АФП. При этом маленькие опухоли
(1 см) визуализируются в виде гиперэхогенных образований, окруженных капсулой.
Следует отметить, что у 25-65 % больных при тщательном обследовании обнаруживаются
опухоли диаметром 2 см и менее.
15. Какая первичная опухоль
печени развивается у молодых людей при отсутствии фонового цирроза?
Фиброламеллярный вариант
гепатоцеллюлярного рака представляет собой особый медленно растущий подтип
рака печени. Средний возраст заболевших — 26 лет.
В анамнезе у пациентов редко
имеются указания на наличие предшествующего заболевания печени. Фиброламеллярная
опухоль, в отличие от наиболее распространенной формы гепатомы, одинаково
часто поражает мужчин и женщин. Она обычно представляет собой крупное единичное
образование, расположенное в левой доле печени (в 75 % случаев). Опухоль
часто вызывает боли в животе. У пациентов отмечается незначительное или
умеренное повышение уровней трансаминаз в сыворотке крови, однако уровень
АФП остается в пределах нормы. Термин "фиброламеллярная" отражает гистологическое
строение опухоли, в которой гепатоциты разделены тонкими слоями фиброзной
ткани. При использовании визуализирующих методов исследования можно выявить
центральный рубец. Распознавание этого варианта гепатоцел-люлярного рака
имеет большое значение, т. к. примерно у половины пациентов опухоль операбельна
на момент постановки диагноза.
16. Какие факторы способствуют
развитию холангиокарциномы? Назовите основные подтипы опухоли.
Холангиокарциномы, на долю
которых приходится 10-20 % всех первичных опухолей печени, развиваются
(как и аденокарциномы) из эпителия желчных протоков. К факторам риска развития
холангиокарциномы относятся первичный склерозиру-ющий холангит, трематодоз
печени, контакт с торотрастом и врожденные кистозные заболевания печени,
такие как болезнь Кароли (Caroli) и кисты холедоха. Наиболее частый симптом
опухоли — желтуха. Возможно также повышение уровней опухолевых маркеров
— СЕА, СА 19-9 или АФП.
В зависимости от локализации
холангиокарциномы делятся на периферические и центральные (расположенные
в области ворот печени) (так называемые опухоли Клацкина [Klatskin]). Периферическая
холангиокарцинома напоминает гепатоцел-люлярный рак, однако, как правило,
не сопровождается циррозом печени. Обычно она гиповаскуляризирована (вследствие
развития склеротической реакции). Опухоли Клацкина образуются в месте слияния
правого и левого печеночных протоков и плохо определяются при визуализирующих
методах исследования. Клиника механической желтухи сопровождается выявлением
выраженного расширения внутри-печеночных желчных протоков при УЗИ и КТ.
К редким вариантам принадлежат холангиоцеллюлярные карциномы, развивающиеся
из каналов Геринга (Hering), и смешанные гепатоцеллюлярные холангиокарциномы,
в которых оба опухолевых компонента существуют рядом или перемешаны.
17. Назовите внешние характеристики,
позволяющие отличать первичные опухоли печени от метастазов.
Различные злокачественные
опухоли печени трудно различимы при УЗИ, КТ или МРТ, однако некоторые признаки
обладают определенным диагностическим значением. Лучшим методом диагностики
считается динамическая болюсная компьютерная томография с предварительным
выполнением неусиленных томограмм. Некоторые врачи для определения объема
хирургического вмешательства предлагают выполнять МРТ. На компьютерных
томограммах большинство метастазов после введения контрастного вещества
определяются в виде очагов низкой плотности (темных) на фоне окружающей
нормальной ткани печени. Они имеют неровные края и более темную центральную
часть (зона некроза). Гиперваскуляризированным метастазам (почечно-клеточные
опухоли, саркомы и карциноиды) свойственно наличие на ранних снимках светящегося
ободка по периферии опухоли (участок повышенной плотности), который в последующем
приобретает нормальную плотность. Таким образом, после дополнительного
контрастирования этот ободок не определяется. В данном случае диагностическую
ценность имеют неусиленные томограммы. Метастазам рака ободочной и прямой
кишки присуща характерная картина на отсроченных КТ, выполненных через
3-5 мин после введения контрастного вещества: участок центрального разрастания
соединительной ткани дает усиление сигнала и окружен опухолью низкой плотности.
Эти изменения соответствуют ультразвуковой картине опухоли, имеющей вид
"яблочка" мишени.
К КТ-признакам гепатоцеллюлярного
рака относится наличие капсулы, отделяющей опухоль от остальной ткани печени,
или очага поражения с неоднородным внутренним строением. Гиперваскуляризация
раковой опухоли делает возможным получение дополнительной информации при
помощи динамической болюсной КТ. В большинстве случаев введение контрастного
вещества вызывает немедленное и равномерное усиление сигнала прежде, чем
произойдет более медленное связывание контрастного вещества клетками опухоли.
Данная методика позволяет также выявить прорастание опухоли в воротную
вену.
Первичные и метастатические
злокачественные образования печени дают одинаковую картину при МРТ: на
Т1-томограммах они определяются как очаги сниженной интенсивности (темные),
а на Т2 — как очаги повышенной интенсивности (яркие). Наибольшую помощь
МРТ оказывает при проведении дифференциальной диагностики гепатоцеллюлярного
рака и доброкачественных гемангиом. Дифференциальную диагностику образований
печени можно также проводить при помощи УЗИ. Однако ультразвуковая картина
во многом определяется гистологическим строением опухоли, что значительно
снижает ценность данного метода.
18. Какая опухоль печени
развивается при длительном контакте с винилхлоридом?
Полагают, что винилхлорид
чаще всего вызывает развитие ангиосаркомы — наиболее распространенной первичной
мезенхимальной злокачественной опухоли печени у взрослых (хотя, как и все
мезенхимальные опухоли, она встречается редко). Ангио-саркома растет из
клеток эндотелия, имеет богатое кровоснабжение и поражает, как правило,
обе доли печени. Быстрый рост и склонность к метастазированию определяют
крайне неблагоприятный прогноз при ангиосаркоме.
19. Какие еще известны
мезенхимальные опухоли печени?
К другим первичным мезенхимальным
опухолям печени относятся рабдомиосарко-ма, фибросаркома и лейомиосаркома.
Недавно описана также эпителиоидная геман-гиоэндотелиома — мезенхимальная
опухоль, поражающая преимущественно женщин среднего возраста и характеризующаяся
медленным ростом.
Особое внимание следует уделить
первичным лимфомам печени, хотя они встречаются реже, чем вторичные поражения
печени при ходжкинских и неходжкинских лим-фомах. Первичная лимфома представляет
собой крупное одиночное образование, в то время как вторичная характеризуется
многочисленными узелками или гепатоме-галией. У 1/3 больных вторичные лимфомы
так диффузно инфильтрируют печень, что при УЗИ, КТ и МРТ она кажется интактной.
20. Назовите противопоказания
к хирургическому лечению первичных злокачественных опухолей печени и метастазов
рака ободочной и прямой кишки.
Резекция печени остается
единственным методом лечения первичного и метастатического рака печени.
По имеющимся данным, гепатоцеллюлярный рак печени операбелен в 9-37 % случаев;
пятилетняя выживаемость больных после операции составляет примерно 30 %
(при отсутствии цирроза). Аналогичные результаты получены после удаления
метастазов рака ободочной и прямой кишки. Противопоказания к хирургическому
лечению:
• Распространение метастазов
за пределы печени.
• Поражение лимфоузлов по
ходу печеночной артерии.
• Декомпенсированный цирроз
при значительном асците.
• Более четырех метастазов
в печени.
• Прорастание гепатоцеллюлярного
рака в нижнюю полую вену, воротную вену или печеночные вены.
• Поражение обеих долей
печени.
21. Какие новые визуализирующие методы
оценки операбельности опухоли разрабатываются в настоящее время?
Успех хирургического вмешательства
зависит от стадии развития опухоли. Недавно разработанные методики, позволяющие
увеличить чувствительность исследования, по-видимому, будут играть важную
роль в будущем. К ним относятся: КТ с липиодо-лом, КТ-портография и интраоперационная
ультрасонография. КТ с липиодолом заключается во введении йодированного
масляного контрастного вещества в печеночную артерию с последующим выполнением
компьютерных томограмм (через несколько дней). Гепатомы не способны выводить
контрастное вещество; это повышает разрешающую способность метода и дает
возможность увидеть на отсроченных снимках даже очень маленькие опухоли.
При КТ-портографии обычное контрастное вещество вводится непосредственно
в систему воротной вены (катетер проводится через верхнюю брыжеечную или
селезеночную артерию). По некоторым данным, чувствительность этой разновидности
КТ выше таковой у традиционного метода на 30-40 %, хотя более низкая специфичность
(доброкачественные образования дают ложноположи-тельные результаты) ограничивает
ее эффективность. Считается, что наиболее точным методом диагностики является
интраоперационное УЗИ, чувствительность которого составляет более 90 %.
22. Назовите два паллиативных метода
лечения неоперабельного гепатоцеллюлярного рака.
Паллиативное лечение гепатоцеллюлярного
рака приносит, как правило, нестойкие и неудовлетворительные результаты.
Системная и внутриартериальная химиотерапия, рентгенотерапия и перевязка
печеночной артерии оказываются недостаточно эффективными у большинства
больных. В настоящее время при неоперабельной опухоли печени рекомендуется
использование двух новых, но уже достаточно изученных методик, которые
значительно увеличивают выживаемость. К ним относятся: (1) трансартериальная
эмболизация артерии, питающей опухоль и (2) чрескожное введение в опухоль
этанола под ультразвуковым контролем. Окончательную оценку эффективности
данных паллиативных вмешательств должны определить длительные контролируемые
исследования.
23. Какие доброкачественные процессы
в печеночной ткани могут симулировать объемные образования печени?
На объемные образования печени,
описанные выше, иногда весьма похожи местная (ограниченная) жировая инфильтрация
и макрорегенеративные узлы (известные также как аденоматозная гиперплазия
или псевдоопухоли). Ограниченная жировая инфильтрация печени часто наблюдается
при алкоголизме, ожирении, сахарном диабете, нарушении питания, повышении
в крови уровня кортикостероидных гормонов (вследствие эндокринных нарушений
или проводимого лечения) и ВИЧ-инфекции. При У ЗИ она определяется в виде
гиперэхогенного образования с четкими контурами, не оказывающего влияния
на близлежащие ткани. Ценность неусиленных компьютерных томограмм невелика,
т. к. ограниченная жировая инфильтрация печени дает достаточно вариабельную
КТ-картину. Сканирование печени с коллоидной серой, меченной радиоактивным
технецием, часто обнаруживает нормальное поглощение в участке инфильтрации.
Для подтверждения диагноза применяется сканирование с ксеноном-133. На
Т1-томограммах отмечается незначительное усиление интенсивности очага инфильтрации
по сравнению с окружающими тканями, а Т2-томограммы ничем не отличаются
от нормальных. Важно отметить, что ограниченная жировая инфильтрация печени
быстро исчезает при успешном лечении основного заболевания. Больше проблем
доставляет диффузная жировая инфильтрация печени с ог-раниченными участками
интактной паренхимы. При УЗИ может выявляться картина нормальной печени,
инфильтрированные жиром ткани способны скрывать метастазы, а интактная
паренхима — имитировать объемные образования. Поэтому для постановки правильного
диагноза необходимо проявить максимум внимания и тщательно изучить картину
заболевания.
У 25 % пациентов с циррозом
печени обнаруживаются макрорегенеративные узлы (участки скопления гепатоцитов
> 1 см в диаметре с интактными портальными трактами). Будучи доброкачественными,
они, однако, могут содержать диспластически измененные гепатоциты и классифицируются
как предраковые состояния по причине их тесной связи с гепатоцеллюлярной
карциномой. Наличие в узлах отложений железа или других гетерогенных включений
указывает на их злокачественную трансформацию. При визуализирующих методах
исследования макрорегенеративные узлы дают разную картину. Основной метод
дифференциальной диагностики узлов и гепатомы — МРТ (с использованием Т2-сигнала).
Макрорегенеративные узлы обычно определяются как образования пониженной
или нормальной интенсивности, в то время как раковая опухоль — как образование
повышенной интенсивности. В силу этих диагностических трудностей необходимо
обязательное выполнение морфологического исследования очага поражения при
помощи тонкоигольной биопсии или аспирации под ультразвуковым контролем,
которое повторяют, если размеры или структура образования изменяются.
24. Каковы подходы к оценке
объемных образований печени?
У пациента с объемным образованием
печени следует проводить тщательную дифференциальную диагностику возможных
заболеваний. Прежде чем применять визуализирующие методы исследования,
требуется изучить клиническую картину и лабораторные изменения, выяснить
наличие фонового заболевания печени или внепеченочных злокачественных опухолей.
Также нужно уточнить, какие лекарственные препараты принимал пациент и
нет ли у него профессиональной вредности. Симптоматические образования
и образования, обнаруженные случайно, чаще всего имеют разную этиологию.
Важными факторами являются также возраст и пол больного. Цирроз печени
требует иного подхода, чем поиск метастазов в печень. Для того чтобы избежать
диагностических ошибок, необходимо знать, как объемные образования могут
проявляться при визуализирующих методах исследования. Случайно обнаруженные
образования. Простые кисты, выявляемые при КТ или МРТ, могут быть верифицированы
при помощи УЗИ. Диагноз гемангиомы, наиболее распространенной доброкачественной
опухоли печени, подтверждает МРТ (если ее размеры < 2,5 см) или исследование
с мечеными эритроцитами. При подозрении на местную узелковую гиперплазию
применяется радионуклидное сканирование печени.
Симптоматические образования.
У
молодых женщин и женщин среднего возраста, принимающих контрацептивные
препараты, необходимо прежде всего подозревать аденому печени, даже если
она протекает бессимптомно. При наличии клинической картины сепсиса предполагаемый
абсцесс печени можно исключить при помощи У ЗИ. Следует помнить, что аналогичным
образом проявляются и первичные опухоли печени. Опухоли. Диагноз
первичной опухоли печени ставится на основании определения уровня АФП,
наличия сопутствующих заболеваний печени и результатов визуали-зирующих
методов исследования. Для оценки метастатической болезни проводится неусиленная
и динамическая болюсная КТ. Выяснение этиологии гиперваскуляризированных
образований иногда требует выполнения ангиографии. В прошлом при подозрении
на гепатоцеллюлярный рак назначали сканирование печени с галлием, однако
данный метод исследования является неспецифическим. Морфологическое
исследование. При подозрении на метастатическую болезнь и для исключения
гепатоцеллюлярного рака, развившегося на фоне цирроза печени, часто выполняют
биопсию образования под ультразвуковым или рентгенологическим контролем.
В 80-90 % случаев диагноз злокачественной опухоли ставится после получения
результатов пункционной биопсии тонкой иглой; при использовании игл от
18 до 22 номера осложнения возникают редко.
У пациентов без цирроза
печени биопсия редко подтверждает диагноз в случае доброкачественного образования
и сопровождается потенциальным риском возникновения кровотечения в случае
богато васкуляризированной злокачественной опухоли печени. Если природа
опухоли неизвестна, а гистологический диагноз имеет большое значение, более
предпочтительно выполнение лапароскопии или лапаротомии и клиновидного
иссечения подозрительного участка (клиновидной биопсии). У сохранных пациентов
во время лапаротомии при необходимости можно выполнить резекцию печени.
При наличии доброкачественного образования и отсутствии показаний к хирургическому
лечению контрольные исследования (УЗИ, КТ, МРТ) необходимо повторять каждые
2-3 месяца для подтверждения отсутствия прогрессирования заболевания.