ГЛАВА 15. ОЦЕНКА ПЕЧЕНОЧНЫХ ПРОБ
1. Что такое печеночные пробы?
Многие лабораторные тесты
можно охарактеризовать как "печеночные пробы". К ним относят такие биохимические
показатели, как аланинаминотрансфераза (АЛТ), аспартатаминотрансфераза
(ACT), гамма-глутамилтрансфераза(ГТТ), щелочная фосфатаза (ЩФ), билирубин
и белки сыворотки крови (в т. ч. альбумин). Эти тесты также иногда называют
функциональными печеночными пробами и печеночными ферментами; однако ни
одно из определений не является абсолютно точным. Лишь первые четыре можно
назвать собственно ферментами, и только два последних отражают собственно
функции печени. Печеночные пробы позволяют охарактеризовать имеющиеся нарушения
и приблизительно оценить синтетическую функцию печени. Эти тесты не являются
в полной мере диагностическими, хотя различные их сочетания полезны в диагностике
специфических заболеваний. Несколько других функциональных печеночных проб
описано ниже. В конечном счете, некоторые тесты помогают выявить специфические
причины заболеваний печени. Ни серологические (например определение антител
к вирусу гепатита С), ни биохимические (например определение уровня альфа1-антитрипсина)
тесты, как правило, не используются для скринингового анализа и планового
диспансерного обследования.
2. Что такое истинные функциональные
печеночные пробы?
Посредством истинных функциональных
печеночных проб оценивают синтетическую функцию печени или ее способность
поглощать различные вещества и удалять их из кровотока, а также метаболизировать
и видоизменять вводимые диагностические препараты. Определение уровня альбумина
— один из наиболее часто используемых в клинике показателей, хотя он и
не является высокочувствительным и на него оказывают влияние недостаточное
питание, заболевания почек и прочие факторы. В целом низкий уровень альбумина
свидетельствует о снижении синтетической функции печени. Определение протромбинового
времени (ПВ) — другой несложный тест, с помощью которого устанавливается
способность печени синтезировать факторы свертывания крови. Изменение протромбинового
времени связано как с нарушением синтезирующей функции печени, так и с
дефицитом витамина К. Увеличение протромбинового времени и отсутствие его
реакции на введение витамина К внутрь (по 5-10 мг в течение 3-х дней) указывает
на заболевания печени или нарушения всасывания витамина К вследствие обструкции
желчного протока или внутрипеченочного холестаза, препятствующих поступлению
желчи в двенадцатиперстную кишку. Подкожное или внутривенное введение витамина
К помогает при дифференциальной диагностике.
Существуют различные тесты
для определения поглотительной и выделительной функций печени; в них используются
такие вещества, как бромсульфофталеин, трикарбоцианиновый краситель, аминопирин,
кофеин, моноацилглицинксилидид. Их часто применяют для оценки тяжести поражений
печени и прогнозирования исхода заболевания в исследовательских целях,
однако в клинической практике к ним прибегают редко.
3. Какова разница между
холестатическим и печеночно-клеточным (паренхиматозным) поражением?
Два основных механизма повреждения
печени — это повреждение или деструкция гепатоцитов (печеночно-клеточный
механизм) и нарушение транспорта желчи (хо-лестатический механизм). Причинами
паренхиматозного поражения печени наиболее часто являются вирусный гепатит,
аутоиммунный гепатит, а также различные токсические вещества и лекарственные
средства. Транспорт желчи нарушается вследствие внепеченочной обструкции
желчных протоков (например желчными камнями или при развитии послеоперационной
стриктуры), сужения внутрипеченочных протоков (например при первичном склерозирующем
холангите), повреждения желчных протоков (например при первичном билиарном
циррозе печени) или нарушения транспорта желчи на уровне мелких желчных
протоков (например при применении хлорпромазина). В некоторых случаях имеют
место оба механизма повреждения. Наиболее специфичный показатель повреждения
паренхимы печени — уровень АЛТ. Уровень ACT также может быть повышен (хотя
данный показатель не столь специфичен). О холестатическом поражении печени,
напротив, с большей вероятностью свидетельствует повышение уровня ЩФ. Желчные
кислоты стимулируют выработку ЩФ, однако закупорка или повреждение желчных
протоков препятствуют ее поступлению в двенадцатиперстную кишку, что приводит
к значительному повышению концентрации ЩФ в сыворотке крови. Уровень ЩФ
незначительно повышен на ранних стадиях поражения печеночной паренхимы.
Однако это происходит вследствие высвобождения фермента из гепатоцитов,
а не стимуляции его синтеза. Поскольку ЩФ вырабатывается и в других органах
(костях, кишечнике), сопутствующее повышение уровней ГГТ и 5'-нуклеозидазы
указывает на холестатический механизм поражения.
4. Что такое сывороточные
трансаминазы? Для чего они используются?
В клинической практике чаще
всего определяют уровень двух сывороточных транс-аминаз - АЛТ и ACT. По
сей день используется, как правило, старая терминология, по которой АЛТ
называется сывороточной глутамат-пируваттрансаминазой, a ACT -сывороточной
глутамат-оксалаттрансаминазой. Новые названия более точно отражают функцию
этих ферментов, заключающуюся в переносе аминогрупп с одного соединения
на другое.
Как отмечено выше, повышение
уровня АЛТ и/или ACT свидетельствует о повреждении гепатоцитов. Необходимо
понять, каким образом выполняются эти тесты и какие факторы способны изменять
их результаты. В большинстве случаев АЛТ определяется с помощью следующей
реакции:
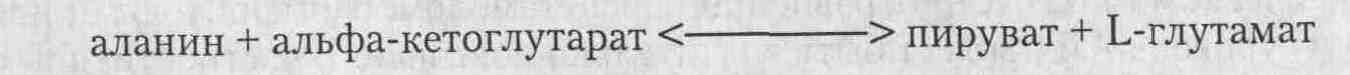
Для этой реакции требуется
наличие АЛТ и пиридоксальфосфата (витамина В6). Важно уяснить,
что с помощью ферментных реакций определяется не собственно уровень
энзима, а (косвенно) его каталитическая активность. Данный анализ
показывает не уровень АЛТ, а скорость катализируемой реакции. Полученный
результат оценивают следующим образом: чем выше скорость реакции, тем больше
количество АЛТ. Недостаток реакции заключается в невозможности определить
количество ее продуктов при повышении уровня АЛТ. Поэтому вместо нее используют
реакцию со связанным ферментом:
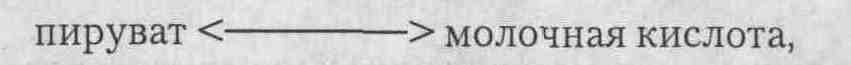
которая проходит в присутствии
другого фермента — лактатдегидрогеназы. В ходе реакции происходит окисление
восстановленного никотинамидадениндинуклеоти-да (Н АДН), а в качестве побочного
продукта образуется его невосстановленная форма (НАД+). НАД+ поглощает
световые волны длиной 340 нм. Поглощение регистрируется при помощи спектрометра
и используется для определения активности АЛТ. В итоге, количество фермента
можно оценить лишь косвенным образом. На скорость реакции влияют несколько
факторов: температура, концентрация веществ, количество ферментов или кофакторов,
наличие тормозящих реакцию примесей, а также чувствительность спектрометра.
Например, если у больного отмечается дефицит пи-ридоксальфосфата, т. е.
его недостаточно для постановки тестовой реакции, скорость ее замедлится,
и в конечном итоге будет получен ложный результат низкой активности АЛТ.
Этот эффект часто наблюдается у алкоголиков (питание которых снижено),
поскольку дефицит витамина В6 приводит к ограничению скорости
реакции в большей степени, чем уровень АЛТ.
Второй спорный вопрос: что
можно считать нормальным уровнем, а что — отклонением от нормы? Это обычно
производится в местной лаборатории произвольным способом, для чего отбирается
небольшая группа "здоровых" пациентов (часто из банка крови), у которых
определяется уровень АЛТ и подсчитывается среднее и стандартное отклонение.
Границы выбираются произвольно; обычно они соответствуют максимальному
и минимальному значениям, которые были получены у 2,5 % отобранной популяции.
Однако подобная методика неудачна, т. к. уровень АЛТ зависит от многих
демографических факторов. У мужчин он выше, чем у женщин. Женщины, страдающие
ожирением, имеют более высокий уровень АЛТ, нежели люди, чей вес близок
к идеальному. У представителей некоторых расовых групп по сравнению с другими
уровень АЛТ также выше. Поэтому, если обследуемая группа пациентов состоит
из худых женщин (особенно европеоидной расы), которым приходилось сдавать
кровь, границы нормы окажутся весьма низкими, в результате у многих мужчин,
страдающих избыточным весом, уровень АЛТ будет высок даже при отсутствии
заболевания. Это характерно для всех ферментативных реакций, описанных
в данной главе. Следовательно, чем больше уровень (скорость) ферментативных
реакций отклоняется от нормы, тем более вероятно наличие заболевания. И
наоборот, у больных с бессимптомным течением заболеваний печени даже при
значительных поражениях паренхимы уровень АЛТ может быть нормальным.
Поэтому уровень АЛТ — недостоверный
маркер патологического процесса в печени. При массивных поражениях печеночной
паренхимы (например при вирусном гепатите, токсическом гепатите — отравлении
парацетамолом, растворителями или мухоморами) уровень АЛТ может быть значительно
повышен. В частности, при сильной передозировке парацетамола значение АЛТ
нередко достигает 2000 ЕД/л (что примерно в 50 раз превышает верхнюю границу
нормы). Это свидетельствует о значительном выходе фермента из поврежденных
гепатоцитов. У больных с хроническим вирусным гепатитом уровень АЛТ, как
правило, превышает нормальные величины в 5-10 раз.
5. Что является причиной
повышения уровня ЩФ?
ТИФ — фермент, катализирующий
перенос фосфатных групп. Различные его изоэнзимы вырабатываются в печени,
костях и кишечнике. В большинстве больничных лабораторий оборудование для
раздельного определения различных форм ЩФ и ее источника отсутствует, что
приводит к некоторым сложностям при диагностике. По данным обследования
большой группы госпитализированных больных, лишь в 65 % случаев высокий
уровень ЩФ был обусловлен заболеваниями печени. Повышение уровня "печеночной"
фракции фермента является следствием стимуляции его синтеза при местном
увеличении концентрации желчных кислот. Это происходит при возникновении
холестаза, вызванного лекарственными препаратами, и при внутри- или внепеченочной
обструкции желчных путей. Тестовая реакция для определения ЩФ:

Обнаружение нитрофенила свидетельствует
о наличии ЩФ. Хотя данная реакция и не связана с ферментом, однако проблемы,
возникающие при определении активности фермента и установлении границ нормы,
аналогичны таковым у сывороточных трансаминаз. Одновременное повышение
уровня ТИФ и гамма-глутамилтранспепти-дазы (или 5'-нуклеозидазы) свидетельствует
в пользу заболеваний печени и указывает на наличие холестаза.
6. Что означает повышение
уровня билирубина?
Билирубин — продукт распада
эритроцитов — существует в двух формах: конъюги-рованной и неконъюгированной.
Неконъюгированный билирубин появляется в плазме, когда скорость разрушения
эритроцитов превышает резервные возможности печени по его трансформации
(что часто встречается у больных с гемолитической анемией). Генетически
обусловленный дефицит некоторых ферментов приводит к тому, что процесс
конъюгации билирубина в печени происходит неправильно или неполно. Наиболее
часто это наблюдается при синдроме Жильбера (Gilbert), который характеризуется
относительным дефицитом глюкуронилтрансферазы и незначительно выраженной
гипербилирубинемией. При голодании или снижении калорийности потребляемой
пищи (например у больных с вирусным гастроэнтеритом) уровень билирубина
в крови повышается в первую очередь за счет его неконъюгированной формы.
Если фракции билирубина не исследуются, больному с болью в животе, тошнотой,
рвотой и гипербилирубинемией может быть ошибочно поставлен диагноз холецистита.
Исследование фракций билирубина помогает избежать выполнения ненужной холецистэктомии
при постановке неправильного диагноза. Чаще всего исследование уровня билирубина
включает биохимическую реакцию с расчетом так называемого избыточного времени.
В большинстве лабораторий определяется только общий билирубин. Количество
непрямого (неконъюгированного) билирубина можно рассчитать, если остановить
реакцию в определенное время и вычесть полученное значение из величины,
определяющей общий билирубин. Точное измерение количества билирубина и
его фракций возможно с помощью хроматографии, оборудование для проведения
которой имеется далеко не во всех лабораториях. Уровень конъюги-рованного
билирубина повышается при многих заболеваниях: вирусном, токсическом, лекарственном
и алкогольном гепатитах, циррозе печени, метаболических нарушениях, обструкции
внутри- и внепеченочных желчных протоков.
7. Какие тесты используются для диагностики
наиболее распространенных метаболических нарушений?
У больных с заболеваниями
печени в плановом порядке применяются специфические лабораторные тесты,
позволяющие выявить некоторые метаболические нарушения. Гемохроматоз
—
заболевание, характеризующееся избыточным отложением железа в печени и
других органах. Скорее всего причиной данного заболевания является нарушение
регуляторного механизма всасывания железа в тонкой кишке. В течение многих
лет его запасы в печени, поджелудочной железе, сердце и других органах
увеличиваются. Чаще всего в качестве скринингового теста при гемохрома-тозе
используют определение уровня сывороточного ферритина. Его повышение указывает
на возможность избыточного содержания в организме железа. Однако уровень
ферритина повышается также в острой фазе воспалительного процесса, поэтому
полученные результаты нередко могут быть ложноположительными. При повышении
уровня ферритина (обычно => 400 мкг/л) необходимо определить уровень сывороточного
железа и железосвязывающую способность (TIBC) крови. Если отношение сывороточного
железа к TIBC превышает 50-55 %, то, вероятнее всего, у больного имеется
гемохроматоз (а не гемосидероз — вторичное избыточное отложение железа
в тканях). Наиболее достоверным является количественное определение железа
в биоптате ткани печени. Затем рассчитывается возрастная поправка, называемая
возрастным индексом железа:
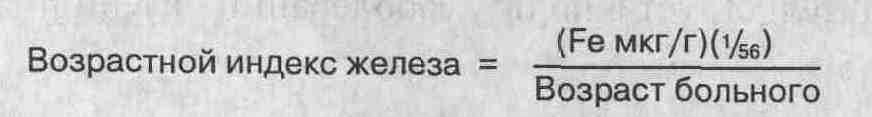
Получены данные, что в установлении
диагноза может помочь магнитно-ядерная резонансная томография. ЯМРТ позволяет
ограничить круг показаний к выполнению биопсии печени.
Альфа1-антитрипсин —
фермент, вырабатываемый печенью, который помогает расщеплять трипсин и
другие тканевые протеазы. Описано множество модификаций (изоформ) этого
фермента, которые зависят от аллелей, полученных от обоих родителей, в
связи с чем у одного человека в крови может обнаруживаться одна или две
формы альфа1-антитрипсина. Z-форма (называемая так из-за ее особой электрофоретической
активности в геле) представляет собой продукт генетической мутации одной
из аминокислот широко распространенного типа белков — М-белка. Z-белок
с трудом высвобождается из клеток печени и вызывает локальные повреждения,
которые могут приводить к гепатиту или циррозу. Поставить диагноз помогают
три теста. Первый — электрофоретическое исследование белков сыворотки (ЭБС).
Под влиянием электрического поля белки крови перемещаются в геле и разделяются;
при этом образуется несколько полос. Одна из них, полоса альфа!, состоит
преимущественно из альфа1-антитрипсина. Поэтому дефицит альфа!-антитрипсина
приводит к ее уменьшению. Второй тест заключается в прямой оценке количества
фермента с использованием моноклональных антител. Степень связывания измеряется
спектрофотометром по методу нефелометрии. Третий способ — определение фенотипа
альфа1-антитрипсина. Лишь в некоторых лабораториях США имеется возможность
выполнить это исследование, направленное на распознавание аллелей протеина,
содержащегося в сыворотке (MM, ZZ, MZ, FZ). У пациентов с протеином типа
ZZ выявляется гомозиготный дефицит альфа!-антитрипсина. Данная форма наиболее
часто сопровождается тяжелыми заболеваниями печени. Если в гепатоцитах
содержится Z-протеин, его можно обнаружить в ткани печени в виде маленьких
глобул, окрашивающихся красителем Шиффа (PAS-положительная реакция) и устойчивых
к воздействию фермента диастазы. В некоторых лечебных учреждениях используется
также реакция иммунофлюорес-ценции.
Болезнь Вильсона (Wilson)
— нарушение усвоения и накопления меди, связанное с дефицитом фермента,
содержащегося в клетках печени. Так же как и железо, медь может откладываться
во многих тканях организма. Тем не менее накапливается она в основном в
определенных местах. Отложения меди обнаруживаются в роговице (кольца Кайзера-Флейшера
(Kayser-Fleischer)) и некоторых отделах мозга. Многие холе-статические
заболевания печени (например первичный билиарный цирроз) также приводят
к избыточному накоплению меди, однако ее отложения никогда не достигают
таких размеров, как при истинной болезни Вильсона. Основной скрининговый
тест — определение уровня церулоплазмина в сыворотке, который снижен у
95 % лиц с болезнью Вильсона. Церулоплазмин является белком острой фазы
воспаления, поэтому его содержание повышается у больных с воспалительными
процессами, у которых его исходный уровень был нормальным или низким. В
процессе наблюдения за больными регулярно оценивается уровень меди в моче
и сыворотке крови. Биопсия печени с последующей количественной оценкой
содержания в ней меди позволяет поставить окончательный диагноз. Отложения
меди в тканях окрашиваются специальными красителями (например роданином).
Диагностические тесты при наиболее
часто встречающихся метаболических нарушениях печени
|
ЗАБОЛЕВАНИЕ
|
ОСНОВНОЙ
ТЕСТ
|
ВСПОМОГА-
ТЕЛЬНЫЙ ТЕСТ
|
ТЕСТ, ПОЗВОЛЯЮЩИЙ
ПОСТАВИТЬ ОКОНЧАТЕЛЬНЫЙ ДИАГНОЗ
|
|
Гемохроматоз
|
Уровень сывороточного
ферритина > 400 мкг/л
|
TIBC >
55
%
|
Возрастной
индекс железа > 2
|
|
Дефицит
альфа1-антитрипсина
|
Электрофорез
белков сыворотки или определение уровня моноклональных антител к альфа
1-антитрипсину
|
Определение
фенотипа (Pi-тип)
|
Биопсия
печени с обнаружением PAS-положительных, диастазо-устойчивых гранул
|
|
Болезнь Вильсона
|
Уровень церулоплаз-мина
< 10 мг/дл
|
Уровень меди
в моче/ сыворотке > 80 мкг/ 24ч
|
Биопсия печени
(количественное содержание меди в ткани > 50 мкг/г)
|
К множеству других наследственных
заболеваний печени относятся болезнь Гоше (Gaucher), болезнь Ниманна-Пика
(Niemann-Pick) и наследственная тирозинемия. Эти редкие заболевания обычно
диагностируются у детей. Специфические диагностические методы исследования
в данной главе не рассматриваются.
8. Что такое аутоиммунные
маркеры? Каким образом они связаны с диагностикой заболеваний печени?
Аутоиммунные маркеры — антитела
к специфическим клеточным компонентам, которые эпидемиологически связаны
с развитием специфических заболеваний печени. К ним относятся антинуклеарные
антитела (ANA), антитела к гладким мышцам (ASMА, также называемые антиактиновыми
антителами), антитела к микросомам печени и почек типа 1 (LKM-1), антимитохондриальные
антитела (AMА), растворимый печеночный антиген (SLA) и антитела к сиалогликопротеиновым
рецепторам. Чаще всего используются тесты для определения ANA, ASMA и АМА;
они позволяют диагностировать наиболее распространенные аутоиммунные заболевания
печени. В настоящее время определение SLA в США не всегда возможно. Антитела
выявляются при помощи следующей реакции: культура клеток обрабатывается
сывороткой больного, после чего образовавшийся комплекс антиген-антитело
(АГ-АТ) "метится" связанными с флюоресцеином человеческими антителами.
Образующийся тройной комплекс обнаруживается при люминесцентной микроскопии.
Разделение клеток осуществляют в соответствии с интенсивностью свечения
и с тем, какая часть клетки связывает антитела. Таким образом, определение
уровня антител и разделение результатов на положительные и отрицательные
весьма субъективно. Большинство гепатологов вносят эти тесты в диагностический
алгоритм только в том случае, если получены положительные результаты при
титрах, больших чем 1 : 80 — 1 : 160. ANA и ASMA чаще обнаруживаются у
пожилых людей, женщин, а также у пациентов с многими другими заболеваниями
печени. Поэтому диагностика аутоиммунного заболевания печени основывается
на общей клинической картине; при этом учитываются возраст, пол больного,
наличие других аутоиммунных процессов, уровни гамма-глобулинов и результаты
биопсии печени. Следует отметить, что при разных аутоиммунных заболеваниях
возможно обнаружение одних и тех же антител. В таблице представлена в общих
чертах одна из классификаций аутоиммунных заболеваний печени. Была также
предложена новая система оценки, в которой авторы постарались учесть факторы,
упомянутые выше.
Классификация аутоиммунных заболеваний
печени
|
ЗАБОЛЕВАНИЕ
|
АНТИТЕЛА
|
|
|
Тип I, классический
люпоидный гепатит
|
ANA и/или
ASMA
|
|
|
Тип II, аутоиммунный
гепатит
|
LKM-1
|
|
|
Тип III,
аутоиммунный гепатит
|
SLA
|
|
|
Первичный
билиарный цирроз
|
АМА
|
|
9. В каких случаях у больных
с подозрением на заболевание печени выполняются скрининговые или диагностические
тесты?
Скрининговые методы исследования,
выполняемые при подозрении на наличие заболеваний печени, включают определение
уровней трансаминаз, билирубина и щелочной фосфатазы. Анамнез, объективное
обследование и оценка факторов риска помогают решить, какие специфические
диагностические тесты требуется проводить в каждом конкретном случае. Иногда
встречаются больные со скрытыми заболеваниями печени, уровень ферментов
у которых составляет норму или незначительно отличен от таковой. У некоторых
пациентов с изолированным повышением уровня энзимов не удается диагностировать
какое-либо заболевание. Как правило, прежде чем приступить к полному (развернутому)
обследованию больного, следует дважды проверить уровень ферментов печени
для исключения лабораторной ошибки. При многих заболеваниях (например гепатите
В и гепатите С) необходимо доказать факт наличия хронического процесса
(когда патологические изменения сохраняются более 6 месяцев) прежде, чем
приступать к лечению или для подтверждения диагноза или определения стадии
болезни планировать выполнение биопсии печени. Обычно стандартный период
выжидания может изменяться в зависимости от выраженности ферментных нарушений
и вероятности обнаружения излечимого процесса. Например, у женщины с повышенным
в 10 раз уровнем трансаминаз, аутоиммунным заболеванием щитовидной железы
в анамнезе и повышенной глобули-новой фракцией имеется, по всей видимости,
обострение ранее нераспознанного аутоиммунного гепатита. Определение аутоиммунного
профиля и ранняя биопсия печени помогут подтвердить это предположение и
своевременно начать лечение стероидными гормонами и другими иммунодепрессантами.