|
|
МЕНЮ
|
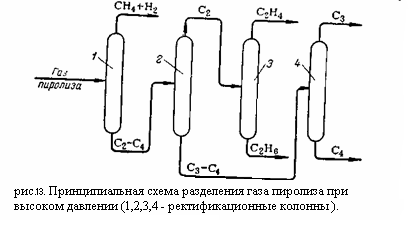
Курсовая работа: Производство этанола методом гидратации этилена1. конденсационно-ректификационный метод (низкотемпературная ректификация), когда разделение газовой смеси – деметанизация, выделение и разделение этан-этиленовой фракции – достигается конденсацией с последующей ректификацией под давлением с применением аммиачного, метанового, этиленового (или пропанового) холодильных циклов. 2. абсорбционно-ректификационный метод, при котором все компоненты тяжелее метана извлекают из газа абсорбцией при низких температурах и затем выделяют низкотемпературной ректификацией. Оба метода требуют затрат холода и применения специальных хладогентов, поскольку критическая температура этилена равна +9,7 °C и ожижение его водой невозможно. Необходимо отметить, что при конденсационно-ректификационном методе основные затраты приходятся на создание низких температур. В связи с этим большое значение имеет эффективность и экономичность применяемых холодильных циклов. Разделение газа пиролиза может осуществляться при низком или при высоком давлении. При разделении при низком давлении (температура ниже -120 °C, давление 1,3 – 2 кгс/см2 ) расширяется интервал температур кипения разделяемых углеводородов и увеличивается их относительная летучесть. Кривая равновесия фаз становится круче, вследствие чего для разделения требуется меньше тарелок, флегмовое число снижается, а чёткость разделения может быть очень высокой. С повышением давления кривая равновесия фаз становится более пологой – увеличивается число тарелок и флегмовое число. Однако для создания низких температур, требуемых для разделения при низком давлении, приходится применять наряду с аммиачным и пропановым также метановый холодильный цикл. Это требует более сложного оборудования и менее экономично, чем этиленовый холодильный цикл, применяемый при высоких давлениях. Вместе с тем, хотя на установках газоразделения при низком давлении получается очень чистый этилен, они малопроизводительны и очень чувствительны к изменению состава газа. Кроме того, их значительно труднее автоматизировать, чем установки высокого давления. 2.3.Разделение пиролиза при высоком давлении При высоком давлении разделение может производиться абсорбционно-ректификационным или конденсационно-ректификационным методами. При использовании конденсационно-ректификационного метода метано-водородная фракция выделяется при температурах от -90 до -100°C, при абсорбционно-ректификационном методе – от -20 до -30°C с использованием лёгкого абсорбента типа фракции С4. Принципиальная схема разделения газа пиролиза при высоком давлении приведена на рисунке 2:
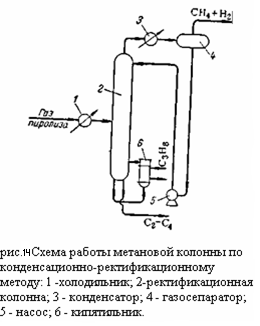
Компримированный, осушенный и охлаждённый газ поступает в метановую колонну 1, где из него выделяются газообразные метан и водород, которые отводятся сверху колонны. Углеводороды С2 – С4 конденсируются в колонне 1 и направляются в этан-этиленовую колонну 2. С верха этой колонны отбирается этан-этиленовая фракция направляемая в этиленовую колонну 3, где этилен и этан разделяется: сверху отбирается концентрированный этилен, а снизу этан. Остаток из колонны 2 представляющий собой смесь из углеводородов С3 – С4, направляется в пропан-пропиленовую колонну 4. сверху из этой колонны отбирается пропан пропиленовая фракция, а снизу бутан-бутеновая. При разделении газа пиролиза при высоком давлении конденсационно-ректификационный и абсорбционно-ректификационный методы различаются в основном лишь схемой и режимами работы метановой колонны. Схема работы метановой колонны при конденсационно-ректификационном методе изображена на рисунке 3:
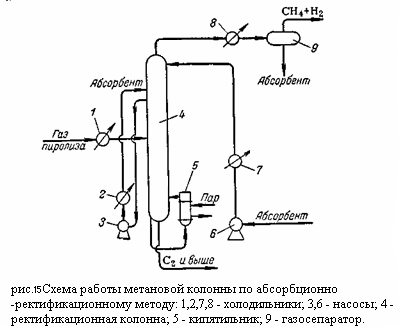
Газ пиролиза в холодильнике 1 охлаждается до минус 55 – 60 градусов Цельсия с использованием аммиачного или пропанового холодильного цикла и поступает в ректификационную колонну 2. Из верхней части колонны 2 (температура вверху минус 95 – 100 градусов Цельсия) отбираются пары метано-водородной фракции, проходящий через охлаждаемый этиленом конденсатор 3, в котором конденсируется часть метана, требуемая для орошения колонны. Конденсат отделяется от паров в газосепараторе 4 и насосом 5 подаётся на орошение колонны 2. Нижняя часть колонны 2 обогревается пропаном с помощью кипятильника 6 (температура внизу колонны 15 – 18 градусов Цельсия). Снизу из колонны выводится смесь углеводородов (С2 и выше), направляемая на дальнейшую ректификацию. При абсорбционно-ректификационном методе метановая колонна (рис.15):
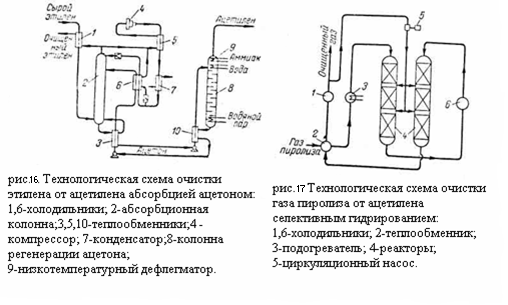
Представляет собой фракционирующий абсорбер (верх колонны работает как абсорбер, а низ – как отпарная колонна). Газ пиролиза перед поступлением в колонну 4 охлаждается в холодильнике 1 до -25°С. Извлечение компонентов тяжелее метана осуществляется путём орашения колонны 4 лёгким абсорбентом (фракция С4 из пропановой колонны), также охлаждённым до -25°С. Расход абсорбента достигает 1,35 кг на кг газа. Необходимость работать с лёгким абсорбентом обусловлена тем, что степень извлечения (абсорбционный фактор) пропорционален числу молей абсорбента: где A – абсорбционный фактор; K – константа фазового равновесия извлекаемого компонента; L, G – количество абсорбента и газа, кмоль. Следовательно, при той же массе абсорбента степень извлечения будет больше для абсорбента с более низким молекулярным весом. Кроме того, для десорбции более лёгкого абсорбента требуются меньшая затрата тепла вследствие более низкой температуры низа десорбера. Недостатком применения лёгких абсорбентов является частичный их унос с отходящими газами, в данном случае с метано-водородными фракциями. Для отвода тепла, выделяющегося при абсорбции, верхняя часть колонны 4 оборудована промежуточными выносными холодильниками 2. уходящая сверху метано-водородная фракция содержит некоторое количество паров абсорбента, зависящее от температуры и давления на верхней тарелке. Для извлечения унесённого абсорбента метано-водородная фракция охлаждается в холодильнике 8 до -60 °С и поступает в ёмкость 9, где газ отделяется от конденсата. Обогрев низа колонны осуществляется через кипятильник 5. однако, поскольку остаток содержит значительное количество абсорбента (фракция С4), температура низа колонны должна быть выше, чем в отсутствии абсорбента, и составляет около 60°C. Соответственно обогрев кипятильника осуществляется водяным паром. Схемы работы колонн 3 и 4 (рисунок 20) такие же, как при конденсационно-ректификационном методе. В режиме этан-этиленовой колонны 2 имеются различия обусловлены большим содержанием абсорбента фракции С4 в остатке. Температура низа этан-этиленовой колонны при работе по конденсационно-ректификационному методу должна быть около 70 °C, в то время как при абсорбционно-ректификационном методе она повышается до 110°C. Соответственно для обогоева кипятильников требуется в первом случае пар низкого, а во втором – высокого давления, при чём расход водяного пара для абсорбционно-ректификационной схемы значительно больше, так как абсорбент циркулирует через все колонны (за исключением этиленовой). Больше также расход воды на охлаждение пропан-пропиленовой колонны. Чистота этилена также получается различной при работе по разным схемам. При одинаковой чёткости разделения в отгонной части метановой колонны абсолютное содержание метана в остатке при работе по схеме с абсорбции будет больше, вследствие того, что количество остатка (фракция С2 – С4 и абсорбент) примерно в три раза больше. Поэтому содержание метана в этилене, полученном абсорбционно-ректификационным методом больше, чем при работе по схеме с конденсацией. Резюмируя, отметим преимущества и недостатки каждого метода. Преимуществами конденсационно-ректификационного метода является меньший расход водяного пара и воды и большая чистота этилена, недостатками – сложность компрессорного оборудования, более низкие температуры и высокие требования к стабильности состава газа. К достоинствам абсорбционно-ректификационного метода относятся умеренно низкие температуры и сравнительная простота эксплуатации; к недостаткам – повышенные энергетические затраты, унос абсорбента и необходимость его выделение при пониженных температурах. По суммарным технико-экономическим показателям предпочтение следует отдать конденсационно-ректификационному методу. Технико-экономические показатели процесса низкотемпературного разделения газа пиролиза определяются, в первую очередь, энергетическими затратами на создание низких температур, а эти затраты в значительной мере зависят от выбранной схемы охлаждения. Охлаждения до низких температур, необходимое для выделения из газа пиролиза, достигается сочетанием методов дросселирования, расширения газа в детандере и каскадного охлаждения за счёт теплообмена с испаряющимся вышекипящим компонентом (например, охлаждение этилена пропаном, метана – этиленом). 2.4. Очистка этилена Очистка этилена сводится к удалению из него сероводорода, двуокиси и окиси углерода, ацетилена и кислорода. Удаление этих примесей может осуществляться на различных стадиях процесса производства этилена. Сероводород, двуокись углерода и органические сернистые загрязнения удаляют путём промывки газо-водной щёлочью (обычно 10% раствором едкого натра) в специальном скруббере. При этом протекают реакции: H2S + 2NaOH → Na2S + 2H2O CO2 + 2NaOH → Na2CO3 + H2O COS + 4NaOH → Na2CO3 + Na2S+ 2H2O CS2 + 6NaOH → Na2CO3+ 2Na2S+ 3H2O Значительное снижение содержания сернистых соединений (до 0,0001%) и двуокиси углерода (до 0,001%) достигается при двухступенчатой промывке щёлочью. Очистка от ацетилена может осуществляться промывкой ацетоном при низких температурах либо, чаще всего, селективным гидрированием. Содержание ацетилена в газе пиролиза колеблется от 0,1 до 1%. При очистке оно должно быть снижено до 0,001 – 0,002 %. Удаление ацетилена абсорбции ацетоном основано на предпочтительном растворении ацетилена в ацетоне и проводится при низких температурах. Охлажденный этилен промывают ацетоном в абсорбционной колонне 2; насыщенный ацетон регенерируется в колонне 8 путём отгона ацетилена и после охлаждения в системе теплообменников и холодильников вновь поступает в абсорбционную колонну 2. Очистка от ацетилена селективным гидрированием основана на реакции: С2Н2 + Н2 → С2Н4 Условия процесса выбираются таким образом, чтобы практически избежать побочной реакции гидрирования этилена. При гидрировании этилен также освобождается от кислорода и от окиси углерода: О2 + 2Н2 → 2Н2О СО + 3Н2 → СН4 + Н2О В качестве катализаторов гидрирования могут применяться никель на кизельгуре, палладий на активированном угле или платина на окиси алюминия. В качестве водосодержащего газа для гидрирования применяется метано-водородная фракция. Гидрирование может проводиться при давлениях 20 - 30 кгс/см2 или более низких и при температуре газа на входе в реактор от 100 до 180 – 200 °C. Избирательное гидрирование ацетилена может проводиться в реакторах трубчатых или колонного типа. В первом случае тепло реакции отводится циркулирующим в межтрубном пространстве сырьём или водой, во втором поддувом холодного гидрированного продукта:
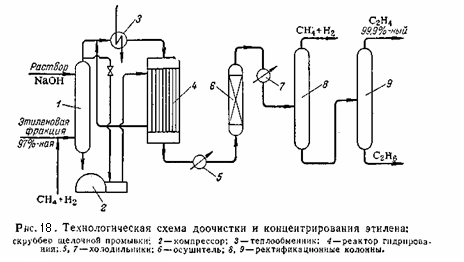
На рисунке приведена технологическая схема очистка газа пиролиза от ацетилена селективным гидрированием. Газ пиролиза после компримирования и осушки проходит теплообменник 2 и паровой подогреватель 3 с температурой 150 - 200°C проходит последовательно реакторы 4 колонного типа. Очищенный газ пиролиза через теплообменник 2 и холодильник 1 направляется на дальнейшее разделение. Часть очищенного газа циркуляционным компрессором 5 подаётся в реакторы 4 для снятия теплоты реакции. Если очистке гидрированием подвергается этиленовая фракция, после гидрирования необходимо концентрирование этилена. Принципиальная технологическая схема доочистки и концентрирования этилена приведена на (рис.18):
Этиленовая фракция (97 – 98 % этилена) смешивается с метано-водородной фракцией и поступает в скруббер 1 для промывки раствором щёлочи с целью удаления углекислого газа, сероводорода и органических сернистых соединений. Отработанная щёлочь выводится снизу, а газ сверху. Газ после щелочной промывки делится на два потока. Один поток проходит межтрубное пространство реактора гидрирования 4 и смешивается со вторым холодным потоком перед паровым подогревателем 3. в паровом подогревателе 3 газ нагревается до 100 – 190 °C и направляется в реактор 4 на гидрирование. Реактор представляет собой трубчатый аппарат, в трубки которого загружен катализатор, например, палладий на активированном угле. Тепло реакции отводится холодной этиленовой фракцией циркулирующей через межтрубное пространство. Давление в реакторе около 23 кгс/см2. После гидрирования газ охлаждается в холодильнике 5 и направляется в осушитель 6 для удаления влаги. Осушенный газ после дополнительного охлаждения в холодильнике 7 направляется в колонну 8 и 9. Сверху из колонны 8 при температуре -38°C отбирается метано-водородная фракция с содержанием этилена до 70%, который возвращается на компримирование. Остаток колонны 8 освобождается от этана в колонне 9. Сверху из колонны 9 при температуре -28°C отбирается 99,9%-ный этилен. Остаток колонны 9 содержит до 60% этана. Температура низа колонны 9 около -20 °C. 2.5. Получение этилена диспропорционированием пропилена Пропилен является побочным продуктом процесса пиролиза на этилен. В связи с этим разработан так называемы процесс «триолефин»,основанная на реакции диспропорционирования пропилена: 2 С3Н6 ↔ С2Н4 + СН3СН=СНСН3
Реакция идёт на окисных катализаторах (Со – Мо или W); в качестве носителя используется окись алюминия. Побочными реакциями являются изомеризация, крекинг и уплотнение: СН3СН=СНСН3 ↔ СН2=СНСН2СН3
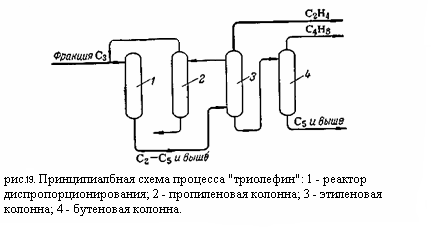
СН3СН=СНСН3 + СН2=СНСН2СН3 → Продукты уплотнения При 500 К равновесная глубина превращения пропилена составляет 45,5 мол.%. Основной причиной понижения выхода в реакции диспропорционирования являются нежелательные реакции изомеризации. Реакции крекинга и уплотнения удаётся подавить подбором условий реакции. Исходный пропилен должен быть очищен от воды, сероводорода, кислорода, кислородсодержащих соединений, метилацетилена и пропадиена. Процесс ведут при 66 – 260 °C, давлении 14 – 41 кгс/см2 и высокой скорости подачи сырья. Реактор периодически останавливают для выжигания кокса, отлагающегося на поверхности катализатора. Количество образующегося кокса составляет всего 0,02 масс.% в расчёте на сырьё, но вследствие большой скорости подачи сырья оно достигает 20% от массы катализатора. Цикл работы между регенерациями колеблется от 20 часов до нескольких суток. Диспропорционирование идёт с большой избирательностью: сумма этилена и бутенов достигает 95 – 97 % от превращённого пропилена, а конверсия пропилена 40 – 45 %. Непрореагировавший пропилен возвращается в реактор. Мольное отношение этилена к бутенам близко к стехиометрическому (около 1:1). Бутен используется для дегидрирования с получением бутадиена-1,3. Принципиальная схема процесса «триолефин» изображена на (рис.19): Пропан-пропиленовая фракция С3 в смеси с рециркулирующим пропиленом поступает в реактор 1 на диспропорционирование. Продукты реакции поступают в нижнюю часть этиленовой колонны 3 из которой сверху отбирается этилен и в виде бокового погона – смесь пропана с пропиленом. Эта смесь направляется в пропиленовую колонну 2, где непревращённый пропилен отгоняется от пропана и возвращается в рецикл. Остаток колонны 3 поступает в бутеновую колонну 4 для отделения высококипящих углеводородов. Из верхней части колонны 4 отбираются бутены высокой чистоты. Процесс «триолефин» позволяет увеличить выход этилена при пиролизе бензина с 26 – 30 до 40,9 % и бутадиена – с 4,7 до 5,7 % при одновременном снижении выхода пропилена с 17,5 до 1,5% и бутенов с 3,5 до 0,4%. [3] 3. ОСНОВНЫЕ МЕТОДЫ ПОЛУЧЕНИЯ СПИРТОВ Спирты применяют в производстве синтетических полимеров, каучуков, пластификаторов, моющих средств, в качестве растворителей и экстрагентов и для других целей. Они являются массовой продукцией нефтехимического синтеза, поэтому большое значение для экономики производства спиртов имеют методы их получения и исходное сырьё. Одним из важнейших методов производства спиртов является гидратация олефинов. Этим методом получают этиловый, изопропиловый, втор- и трет-бутиловые спирты. Метиловый спирт получают на основе окиси углерода и водорода. Наиболее крупнотоннажным продуктом является этиловый спирт. На основе этилового спирта в конце тридцатых годов С.В. Лебедевым был разработан метод получения бутадиена-1,3 и синтетического каучука на его основе. Этиловый спирт получают из пищевого сырья (ферментативный метод), из продуктов гидролиза древесины, из сульфитных щелоков и этилена. Трудовые и сырьевые затраты при производстве этилового спирта из пищевых продуктов и древесных опилок очень велики, поэтому значительно выгоднее исходить из дешёвого углеводородного сырья и получать спирт гидратацией этилена. Для производства одной тонны этилового спирта на основе этилена необходимо переработать всего примерно 2,5 тонны газа или нефтяных дистиллятов, а для получения 1 тонны спирта из растительных материалов требуется 4 тонны зерна, 10 – 12 тонн картофеля или 8 тонн древесных опилок. Трудовые затраты в человеко-часах при производстве этанола из разных источников составляют: из картофеля 280, из зерна 160, из этилена 10. Для получения синтетического этанола сырьём служит этилен, который подвергают сернокислотной гидратации или гидратации на твёрдых фосфорно-кислотных катализаторах (прямая гидратация): С2Н4 + Н2SO4 → C2H5OSO3H + H2O → C2H5OH + Н2SO4; С2Н4 + H2O (H3PO4) → C2H5OH. Себестоимость синтетического этилового спирта значительно ниже, чем при других методах его получения. Относительная себестоимость (в %) этанола, получаемого разными способами, составляет: из этилена 100%, гидролизом древесины 174 – 290, из пищевого сырья 300 – 400. [2] 4. ПРОИЗВОДСТВО СПИРТОВ СЕРНОКИСЛОТНОЙ ГИДРАТАЦИЕЙ ОЛЕФИНОВ 4.1. Теоретические сведения Реакция присоединения воды была открыта Фарадеем 1825 – 1828 гг. он нашёл, что при действии серной кислоты на этилен, содержащийся в светильном газе, наряду с диэтиловым эфиром и другими продуктами образуется этиловый спирт. Впоследствии было установлено, что первым продуктом присоединения серной кислоты к этилену является этилсерная кислота, которая при гидролизе превращается в этанол. В 1873 году А.М.Бутлеров и В.Горяинов детально изучили сернокислотную гидратацию этилена и предсказали техническое значение этого процесса. В начале тридцатых годов в Советском Союзе М.А.Далиным с сотр. были проведены исследования сернокислотной гидратации олефинов и в 1936 году в Баку была создана первая промышленная установка по получению этилового спирта из нефтяных газов. Сернокислотная гидратация олефинов является обратимым процессом. Она протекает в две стадии: CH2=CH2 + Н2SO4 ↔ CH2OSO2OHCH3 + H2O ↔ CH2OHCH3+ Н2SO4 |
Copyright © 2012 г.
При использовании материалов - ссылка на сайт обязательна.