|
|
МЕНЮ
|
Курсовая работа: Биосинтез аминокислотКурсовая работа: Биосинтез аминокислотСОДЕРЖАНИЕ Введение 1. ХАРАКТЕРИСТИКА АМИНОКИСЛОТ. 2. ПРОДУЦЕНТЫ АМИНОКИСЛОТ. 3. БИОСИНТЕЗ АМИНОКИСЛОТ. 3.1 Одноступенчатый метод получения аминокислот. 3.2 Двухступенчатый метод получения аминокислот. 3.3 Получение лизина. 3.4 Получение аминокислот с помощью иммобилизованных ферментов и клеток. 3.5 Технология получения глутамата. 4. ПРОМЫШЛЕННЫЙ СИНТЕЗ АМИНОКИСЛОТ. 4.1 Микробиологический синтез. 4.2 Химический синтез. 5. ПРИМЕНЕНИЕ АМИНОКИСЛОТ. Заключение. Список использованных источников. Введение Современный уровень развития биотехнологии обусловлен общим прогрессом науки и техники, особенно - в течении последних 50 лет. Достаточно отметить лишь такие события, как установление структуры и функций нуклеиновых кислот, обнаружение ферментов рестрикции ДНК и выявление их значения в жизни клеток с последующим использованием в генно - инженерных работах, создание гибридом и получение моноклональных антител, внедрение ЭВМ и компьютерной техники в биотехнологические процессы. Промышленный биосинтез аминокислот относится к микробиотехнологии. По сути своей микробиотехнология тождественна промышленной (технической) микробиологии. Ее объектами являются микробы - вирусы ( включая вироиды и фаги ), бактерии, грибы, лишайники, протозоа. В ряде случаев биообъектами являются первичные метаболиты микробного происхождения - ферменты, каталитическая активность которых лежит в основе инженерной энзимологии. В сравнении с растительным и животным клеткам микробы размножаются, как правило, быстрее и, следовательно, у них быстрее протекают все метаболические (обменные) процессы. Относительные преимущества большинства микробов как биообъектов следующие: 1) большая « простота» организации генома, 2) достаточно легкая приспособляемость (лабильность) к среде обитания в естественных и искусственных условиях, 3) выраженные скорости протекания ферментативных реакций и нарастания клеточной массы в единицу времени. Первое преимущество обеспечивает микробным клеткам лучшие возможности для измерения и перестроек наследственного материала, например, включение в него чужеродной генетической информации, привнесение в клетки или, напротив, элиминации из них плазмид. Второе преимущество, связанное с лабильностью микробов, можно показать на примере бактерий и грибов. Так, применительно к температуре микробы подразделяются на психофилыу мезофиллы и термофилы.[1] 1. ХАРАКТЕРИСТИКА АМИНОКИСЛОТ. Аминокислоты играют большую роль в здравоохранении, животноводстве и легкой промышленности. По значению для макроорганизма аминокислоты подразделяют на заменимые и незаменимые. К незаменимым относятся те аминокислоты, которые не синтезируются в животном или человеческом организме, они должны быть привнесены с пищей или кормом для животным (табл. 1 ). Таблица 1 Заменимые и незаменимые аминокислоты.
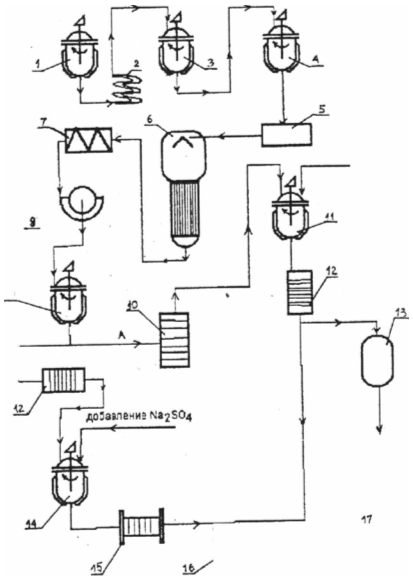
Заменимые синтезируются in vivo из аммиака и различных источников углерода. Микроорганизмы сами синтезируют все необходимые им аминокислоты из аммиака и нитратов, а углеродные « скелеты » - из соответствующих интермедиаторов. Исходя из оценки аминокислот, ученые давно стремятся использовать способности микроорганизмов продуцировать заменимые и незаменимые аминокислоты в ощутимых количествах. Потребность людей в аминокислотах достаточно велика и этим определяется уровень их производства в мире (порядка 500 тыс. тонн в год). Большинство микроорганизмов и зеленые растения способны синтезировать de novo все двадцать аминокислот. Углеродные скелеты аминокислот образуются из промежуточных продуктов обмена. Исходным материалом для синтеза аминокислот служат простые промежуточные продукты катаболизма (пируват, 2 - оксиглутарат, оксалоацетат и фумарат, эригрозо - 4 - фосфат, рибозо - 5 - фосфат и АТР ). При синтезе большинства аминокислот аминогруппа вводится только на последнем этапе путем трансаминирования. Некоторые аминокислоты образуются в результате ряда превращений других аминокислот, и в этих случаях трансаминирование не требуется. Белки синтезируются на рибосомах из аминокислот по информации м - РНК, которая переписана (путем транскрипции ) с генов ДНК.[1,5] 2. ПРОДУЦЕНТЫ АМИНОКИСЛОТ Специфические ферменты, регулирующие биосинтез аминокислот, широко распространены у бактерий; они с определенной глубиной изучены у Escherichia coli. Salmonella typhimurium, Bacillus subtilis и прочие. У грибов, на аминокислотное лимитирование, отмечается некоординированное, параллельное возрастания уровня ферментов, катализирующих реакции биосинтеза различных аминокислот. Этот « общий контроль биосинтеза аминокислот » был также назван « метаболическим интерблоком », или « перекрестнопутевой регуляцией », впервые выявленной у Neurospora crassa в 1965 году М. Карсиотисом и сотрудниками, а позднее - у Saccharomyces cerevisiae, Aspergillus nidulas и других грибов. В гиперпродукции отдельных аминокислот культурами Escherichia coli, Serratia marcescens и другие важную роль играют Feedak - репрессия, например, при биосинтезе ароматических аминокислот на последних стадиях. В любом живом организме аминокислоты расходуются прежде всего на биосинтез первичных метаолитов - ферментных и неферментных белков. Следовательно, кроме биосинтеза аминокислот de novo, возможен другой путь их получения, а именно - из гидролизатов соответствующих белков ( триптофан разрушается при кислотном гидролизе ), в том числе из нативной биомассы микробных клеток. Природные аминокислоты являются, как правило, оптически активными L - и D - формами, которые трудно разделить. Вот почему микробный синтез с помощью коринебактерий и некоторых других микробов является ныне основным и экономически выгодным. Первое место здесь по праву занимает Япония, где лишь глутаминовой кислоты изготавливается свыше 100 тысяч тонн в год; большинство природных незаменимых аминокислот производит фирма «Такеда». С. Киношита, впервые в 50-е годы открывший и доказавший перспективность микробного синтеза, уже 1963 году признавал: «Мало сомнения в том, что недалеко то время, когда с помощью микроорганизмов будет возможно производить все известные аминокислоты». Это время наступило уже к 70 -м годам. Получены микробы - суперпродуценты из родов Brevibacterium, Corynebacterium, Micrococcus и другие, с помощью которых освоено крупнотоннажное производство не только глутамата, но и L - лизина, L - валина, L - гистидина и других. При суперпродукции уровень экспрессии клонированного гена выражается в синтезе специфического белка в количестве 2 % от всех растворимых белков клетки - хозяина. В настоящее время имеются продуценты, у которых количество синтезируемого специфического белка достигает 10-15% (здесь важнейшую роль играют многокопийные плазмиды, несущее встроенный гены). Генно - инженерными методами во ВНИИ генетики и селекции промышленных микроорганизмов ( Москва ) был получен штамм Escherichia coli, обладающий сверхпродукцией L - треонина (30 г / л за 40 часов ферментации ). С любым штаммом - продуцентом какой - либо аминокислоты необходимо внимательное и бережное обращение в целях поддерживания ее в активном состоянии в течении длительного времени. Получен штамм Escherichia coli, продуцирующий за 48 часов 27 г / л L - пролина, и штамм, продуцирующий до 22,4 г / л L - фениланина. С помощью Corynebacterium sp. можно получигь алкапосодержащих средах L - тирозин (до 19 г/л ); с помощью Corynebacterium glutamicum на глюкозной среде - L - валин (до 11 г / л; L - аргинин, L - гистидин, L - изолейцин - 15 - 20,8 г / л. 3. БИОСИНТЕЗ АМИНОКИСЛОТ Технология получения аминокислот базируется на принципах ферментации продуцентов и выделении вторичных метаболитов, то есть размножают маточную культуру вначале на агаризованной среде в пробирках, затем - на жидкой среде в колбах, инокуляторах и посевных аппаратах, а затем в головных (основных ) ферментаторах. Обработку культуральных жидкостей и выделение аминокислот проводят по схеме, аналогичной схеме получения антибиотиков. Изолированные чистые кристаллы целевого продукта обычно высушивают под вакуумом и упаковывают. 3.1 Одноступенчатый метод получения аминокислот Известны два способа получения аминокислот: одноступенчатый и двухступенчатый. Согласно первому способу, например, мутантный полиауксотрофный штамм - продуцент аминокислоты культивируют на оптимальной для биосинтеза среде. Целевой продукт накапливается в культуральной жидкости, из которой его выделяют согласно схеме на рисунке d
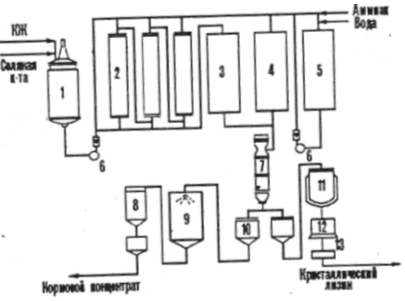
1 - ферментатор, 2 - охладитель, 3,9 - рефрижераторы, 4 - емкость для предварительной обработки, 5 - центрифуга, 6 - вакуум - упариватель, 7 - аппарат прямой 8 - барабанный фильтр, А,Б - пути ( при необходимости смыкающиеся ), 10 - аппарат для ультрофилырации, 11 - емкость для консервации раствора фермента, 12 - мембранный фильтр, 13 - накопитель жидкого консерванта, 14-емкость для осаждения фермента, 15 - фильтр - пресс, 16 - распылительная сушилка, 17 - накопитель сухого концентрата. Рисунок №1 Примерная технологическая схема получения аминокислот. 3.2 Двухступенчатый метод получения аминокислот В двухступенчатом способе микроб - продуцент культивируют в среде, где он получается и синтезирует все необходимые ингредиенты для последующего синтеза ( в идиофазу ) целевого продукта. Если ферменты биосинтеза аминокислоты накапливаются внутриклеточно, но после 1 - ой ступени клетки сепарируют, дезинтегрируют и применяют клеточный сок. В других случаях для целей биосинтеза целевых продуктов применяют непосредственно клетки. 3.3 Получение лизина Если аминокислота предусмотрена в качестве добавки к кормам, то биотехнологический процесс кормового продукта включает следующие стадии: ферментацию, стабилизацию аминокислоты в культуральной жидкости перед упариванием, вакуум - упаривание, стандартизацию упаренного раствора при добавлении наполнителя, высушивание и упаковку готового продукта, в котором должно содержатся не более 10 % основного вещества. Например, в промышленности изготавливают сухой кормовой и жидкий кормовой концентраты лизина наряду с кристаллическим лизином.(рис. 2) Рисунок №2
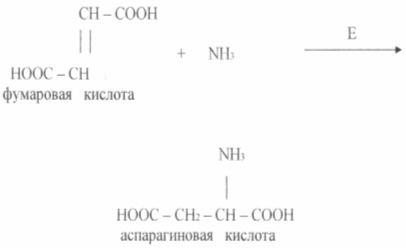
1 - емкость для культуральной жидкости (КЖ), 2 - ионообменные колонны, 3 - сборник злюата, 4 - сборник фильтрата, 5 - емкость для элюата, 6 - насос, 7 - вакуум - выпарной аппарат, 8 - циклон, 9 - сушилка кормового концентрата, 10 - сборник, 11 - реактор - кристаллизатор, 12 - центрифуга, 13 - сушилка. Если концентрат содержит 70 - 80 % сухих веществ, то достаточно устойчив против микробной порчи за счет повышенной осмотической концентрации ингредиентов.[5] 3.4 Получение аминокислот с помощью иммобилизованных ферментов и клеток Экономически целесообразным являются способы получения аминокислот с помощью иммобилизованных ферментов и клеток. Сравнительно давно реализован процесс получения L - аспаргиновой кислоты из фумаровой и аммиака в одну стадию с помощью иммобилизованных клеток Е. coli или Pseudomonas aeruginosa, обладающая аспартазной активностью (см схему)
Аспартаза катализирует реакцию присоединения аммиака к фумаровой кислоте. Фермент в иммобилизованном состоянии сохраняет активность на исходном уровне 2 -2,5 недель и более. L - Аспаргиновую кислоту можно получить и с помощью иммобилизованных клеток, что существенно повышает длительность функционирования системы, производительность которой по целевому продукту составляет около 2000 кг с 1м реактора. Периодические ферментации используют при получений других L - аминокислот (глутаминовой, фенилаланина, лизина, триптофана и др. ). При этом культивируют обычно специальные мутантные штаммы, метаболизм которых по целевому продукту изучен достаточно полно. Так, например, установлено, что лимитирующем агентом коринебак герий, образующих глутаминовую кислоту, является биотип в дозе 1 - 5 мкг/ л. Биотин индуцирует структурно - функциональные изменения в клеточной мембране, благодаря чему увеличивается ее проницаемость для глутаминовой кислоты, выходящей из клетки в культуральную жидкость. Отдельные штаммы продуцентов способны накапливать ее более 50 г/л на мелассных средах. Роль биотина аналогична в случае получения пролина, являющимся производным глутаминовой кислоты. Несложность этой технологии и ее преимущества по сравнению с глубинной ферментацией наглядно иллюстрируют опыт японской фирмы «Танабе Сейяку ». В 1973 году эта фирма разработала способ получения аспарагиновой кислоты при помощи иммобилизованных бактериальных клеток, обладающих аспартазной активностью. Аспартаза катализирует присоединение аммиака по двойной связи фумаровой кислоты, т.е. аспарагиновая кислота образуется в одной стадии и данный биотехнологический процесс можно отнести к категории биотрансформации органических соединений. Иммобилизованный в геле фермент функционировал хорошо, длительность его полуинактивации составила 1 месяц. Затем в геле иммобилизовали клетки продуцента, дополнительно стабилизируя их путем химического связывания между собой и с гелем. Длительность полуинактивации клеток в этом случае увеличивалась до 4 месяцев. Технологию биотрансформации фумаровой кислоты, таким образом, можно представить в такой последовательности: выращивание клеток методом глубинной ферментации и их выделение центрифугированием; иммобилизация клеток биокатализатора в геле в виде гранул размером 2 -3 мм; биотрансформация фумарата аммония в колонке с катализатором в проточном режиме и получение раствора аспарагиновой кислоты; кристаллизация, центрифугирование и промывка кристаллов. Производительность системы биотранеформации аспарагиновой кислоты 1 м биореактора 1700 кг. 3.5. Технология получения глутамата. В основе сверхсинтеза глутаминовой кислоты из глюкозы у этих бактерий лежат два биохимических принципа: недостаток фермента а - кетоглутаратдегидрогеназы и блокировка биосинтеза биотина. Неспособность клеток синтезировать биотин приводит к увеличению проницаемости цитоплазмотической мембраны, что повышает экскрецию глутамата. Он образуется в результате аминирования а - кетоглутарата, неспособного к дальнейшим превращениям в цикле трикарбоновых кислот. Схема биосинтеза глутамата из глюкозы у данного типа мутантов показана на рис. 3 При биосинтезе глутаминовой кислоты очень большое значение имеет концентрация биотина в среде. Необходимо обеспечить его концентрацию 1 - 5 мкг /л. В этом случае нарушается нормальный синтез фосфолипидов мембраны и последняя становится проницаемой для глутамата. При концентрации биотина 15 мкг/л наблюдается интенсивный рост биомассы. Проницаемость цитоплазмотической мембраны для глутамата можно снизить также при помощи пенициллина, добавляя его к среде во время логарифмической фазы роста. В этом случае фосфолипиды экстрагируются из мембраны и транспорт глутамата может осуществляться в течение 40 - 50 часов. Бактериальный синтез глутамата позволяет получать примерно 50 % - ный выход продукта из сахара и накапливать в среде ферментации до 200 г/л глутамата. Известны методы получения глутамата на этанольных средах ( до 60 г/л ) или на ацетате (до 98 г/ л ).[6] Страницы: 1, 2 |
Copyright © 2012 г.
При использовании материалов - ссылка на сайт обязательна.